
Vol. 36, n.º 2, 2003
REVISTA
ESPAÑOLA DE
Vol. 36, n.º 2, 2003 |
Noemi Vidal1, M.ª José Paules1, Carles Villabona2, José Manuel Gómez2, Isidre Ferrer1
Servicio de Anatomía Patológica1 y Endocrinología2, Ciutat Sanitària i Universitària de Bellvitge, l’Hospitalet de Llobregat, España. iferrer@sakma.es
RESUMEN
Introducción: Las cromograninas son proteínas extensamente distribuidas en el sistema neuroendocrino, y su expresión puede usarse en la caracterización de los tumores neuroendocrinos.
Material y métodos: Este estudio analiza mediante inmunohistoquímica la presencia de cromogranina A en 32 biopsias de adenomas hipofisarios humanos, secretores y no secretores.
Resultados: Todos los adenomas secretores de FSH y los no secretores muestran inmunoreactividad intensa para cromogranina A, mientras que otros adenomas hipofisarios son negativos o débilmente positivos en escasas células.
Conclusiones: La cromogranina A puede utilizarse como marcador de adenomas hipofisarios humanos no secretores.
Palabras clave: cromogranina A, hipófisis, adenoma.
SUMMARY
Introduction: Chromogranins are proteins found widely distributed in the neuroendocrine system; their expression can be used in the identification of neuroendocrine tumours.
Material and methods: 32 biopsies of secreting and non-secreting human benign pituitary adenomas were studied by immunohistochemical techniques.
Results: All FSH-secreting and non-secreting adenomas showed strong chromogranine A immunoreactivity, while other pituitary adenomas were negative or only weakly positive in a few scattered cells.
Conclusion: Chromogranin A can be used as a marker of non-secreting human benign pituitary adenomas.
Key words: chromogranin A, pituitary, adenoma.
INTRODUCCIÓN
Las cromograninas/secretograninas (graninas) son una familia de proteínas secretoras acídicas extensamente distribuidas por todo el sistema neuroendocrino en gránulos secretores, donde son almacenados y secretados junto con hormonas peptídicas, aminas y neurotransmisores peptídicos. Las graninas incluyen la cromogranina A (CgA), la cromogranina B (CgB), y la secretogranina II (SgII) (1,2).
La CgA es una proteína de 439 aminoácidos codificada por el cromosoma 14; el gen humano de la CgA es muy similar a los genes murino y bovino de la CgA (3).
La médula adrenal es el lugar de mayor producción y almacén de CgA; la hipófisis contiene un 25% del total; el páncreas, el estómago y el intestino 5% cada uno; las glándulas endocrinas restantes representan menos del 1%. La CgA también se ha hallado en células neuroendocrinas aisladas en muchos otros órganos (mama, pulmón, corazón y próstata) (4).
La función de las graninas no es del todo conocida. Participan en muchas actividades (1,4), como: a) Inhibición enzimática: la CgA inhibe la rotura proteolítica de prohormonas por proteasas o tripsina; b) Precursoras de péptidos funcionales: CgA, CgB y secretogranina II pasan por un proceso proteolítico. En el caso de la CgA, sus fragmentos biológicamente activos incluyen pancreastatina, granina, parastatina, y vasostatina (1,5); c) Almacén de catecolaminas. La CgA participa en el almacenaje de hormonas en vesículas secretoras. La CgA junto a otras proteínas sinápticas, tiene un papel importante en la biogénesis de gránulos secretores, incluso en ausencia de hormonas (6).
La CgA es un marcador útil en suero y tejido de tumores neuroendocrinos, incluyendo feocromocitomas, neuroblastomas, carcinoides, y carcinoma de tiroides; la concentración de CgA está aumentada en pacientes con adenomas no secretores y en algunos adenomas hipofisarios secretores (7).
Este estudio examina mediante inmunohistoquímica la presencia de CgA en una serie de adenomas benignos pituitarios humanos. Los resultados sugieren que la determinación de CgA es un marcador útil del origen endocrino de los adenomas secretores de FSH y, más importante para la clínica, de los adenomas no secretores.
MATERIAL Y MÉTODOS
Muestras de tejido de 32 biopsias de adenomas hipofisarios humanos fueron clasificados según criterios hormonales: 7 no secretores, 7 secretores de ACTH, 3 secretores de PRL, 4 secretores de GH, 6 secretores de GH/PRL, 4 secretores de FSH y 1 secretor de GH/ACTH.
La clasificacion patológica se basó en la inmunohistoquímica realizada en secciones de tejido fijado en formol y parafinado, de 5 m de grosor, procesada con el método avidina-biotina-peroxidasa (ABC, Vector, Vectastain). La inmunohistoquímica se realizó con un teñidor automático (Dako-Biotech Techmate 500) usando anticuerpos monoclonales para ACTH, PRL, LH, FSH, TSH y CgA, y anticuerpos policlonales para GH (todos de Dako). La inmunoreactividad para CgA se clasificó en cuatro grados según el porcentaje de células que mostraban positividad para CgA: +++ Ž75% células, ++ 10-75%, +<10%, – ausencia de positividad.
De los 32 pacientes estudiados 17 eran mujeres y 15 hombres, con edades entre los 22 y los 76 años. Los estudios clínicos incluyeron determinación de niveles hormonales serológicos. Clínicamente los diagnósticos eran: 6 enfermedad de Cushing, 9 acromegalia, 3 prolactinoma, 5 gonadotropinoma y 9 no funcionantes.
RESULTADOS
La inmunoreactividad para CgA se caracteriza por ser granular y citoplasmática, ya que se localiza en los gránulos secretores (fig. 1).
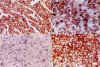
Fig. 1: Las imágenes
corresponden a un adenoma secretor de FSH (A, B) y un adenoma productor de ACTH
(C, D). A y C son tinciones inmunohistoquímicas frente a Cromogranina A.
Destaca la fuerte inmunoreactividad para cromogranina A en el adenoma secretor
de FSH (A), comparado con las escasas células positivas en el adenoma ACTH (C).
Cortes de parafina con hematoxilina, x 400 aumentos.
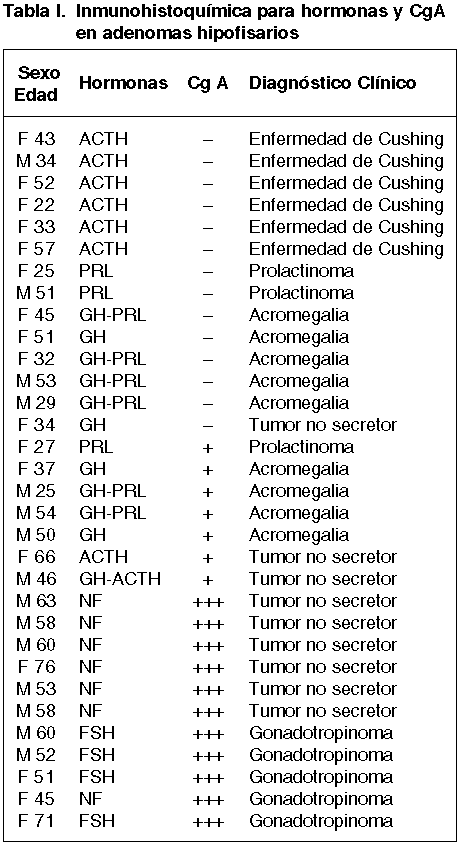
Se encontró positividad fuerte para CgA (+++) en 11 adenomas: 7 no secretores y 4 secretores de FSH. Se hallaron células aisladas positivas para CgA (+) en 7 tumores: 2 GH, 1 GH-ACTH, 2 GH-PRL, 1 PRL y 1 ACTH. La inmunoreactividad fue negativa para CgA (–) en los 14 adenomas secretores restantes. Los resultados están recogidos en la tabla I. En resumen, se halló inmunoreactividad fuerte para CgA en todos los adenomas no secretores y en todos los adenomas secretores de FSH. Los otros adenomas secretores eran negativos o mostraban positividad para CgA en pocas células aisladas.
DISCUSIÓN
Las gonadotropinas (LH, FSH) son sintetizadas en el lóbulo anterior de la hipófisis por un solo tipo de células llamadas gonadotropas (Gn-cell). Se han descrito dos tipos de gránulos secretores en las gonadotropas de la rata macho: uno pequeño que es electrón-denso, y otro mayor y menos electrón-denso. La CgA y SgII son marcadores útiles para discriminar entre los gránulos grandes y pequeños de las gonadotropas en la rata macho ya que la CgA se localiza en los gránulos mayores, y la SgII se halla en los gránulos de menor tamaño (4,8,9). Aunque las graninas tienen un papel crucial en la formación de gránulos secretores en ambos sexos (9,10), se han encontrado diferencias en la inmunoreactividad para CgA y SgII entre ratas macho y hembra (8). Las cromograninas son especialmente útiles como marcadores de los distintos fenotipos de gonadotropas (11).
Estudios previos han mostrado inmunoreactividad para CgA en adenomas hipofisarios (2,12,13), y en muchos tumores neuroendocrinos (13). Aunque las graninas están coalmacenadas con hormonas peptídicas y neuropéptidos en los gránulos secretores, incluso los tumores que carecen de hormonas peptídicas (p.e. adenomas hipofisarios no secretores) contienen graninas como componentes de la matriz densa. Además, estudios actuales y previos con inmunohistoquímica e inmunoescintigrafía en adenomas hipofisarios humanos (14), han mostrado la expresión de CgA concretamente en adenomas hipofisarios no secretores y en secretores de hormonas glicoproteicas. Todos estos datos, así como nuestros resultados indican que la inmunohistoquímica para CgA es un marcador de adenomas gonadotropos, y, más importante para el uso en clínica, un instrumento excelente para demostrar el origen endocrino de los adenomas hipofisarios no funcionantes (15).
BIBLIOGRAFÍA
Huttner WB, Gerdes HH, Rosa P: The granin (chromogranin/secretogranin) family. Trends Biol Sci 1991; 16: 26-30.
Deftos LJ, O’Connor DT, Wilson CB, Fitzgerald PA: Human Pituitary Tumors Secrete Chromogranin-A. J Clin Endocrinol Metab 1989; 68: 869-72.
Canaff L, Bevan S, Wheeler DG, Mouland AJ, Rehfuss RP, White JH, Hendy GN: Analysis of Molecular Mechanisms Controlling Neuroendocrine Cell Specific Transcription of the Chromogranin A Gene. Endocrinology 1998; 139: 1184-96.
Winkler H and Fischer-Colbrie R: The Chromogranins A and B: The first 25 years and future perspectives. Neuroscience 1992; 49: 497-528.
Eskeland NL, Zhou A, Dinh TQ, Wu H, Parmer RJ, Mains RE, O´Connor DT: Chromogranin A Processing and Secretion. Specific Role of Endogenous and Exogenous Prohormone Convertases in the Regulated Secretory Pathway. J Clin Invest 1996; 98: 148-56.
Majó G, Ferrer I, Marsal J, Blasi J, Aguado F: Immunocytochemical analysis of the synaptic proteins SNAP-25 and Rab3A in human pituitary adenomas. Overexpression of SNAP-25 in the mammosomatotroph lineages. J Pathol 1997; 183: 440-6.
Ischia R, Gasser RW, Fischer-Colbrie R, Eder U, Pagani A, Cubeddu LX, Lovisetti-Scamihorn P, Finkenstedt G, Laslop A, Winkler H: Levels and molecular properties of secretoneurin-immunoreactivity in the serum and urine of control and neuroendocrine tumor patients. J Clin Endocrinol Metab 2000; 85: 355-60.
Watanabe T, Azuma T, Banno T, Jeziorowski T, Ohsawa Y, Waguri S, Grube D, Uchiyama Y: Immunocytochemical localization of Chromogranin A and Secretogranin II in Female Rat Gonadotropes. Arch Histol Cytol 1998; 61: 99-113.
Watanabe T, Banno T, Jeziorowski T, Ohsawa Y, Waguri S, Grube D, Uchiyama Y: Effects of Sex Steroids on Secretory Granule Formation in Gonadotropes of Castrated Male Rats with Respect to Granin Expression. Endocrinology 1998; 139: 2765-73.
Gorr SU: Differential Storage of Prolactin, Granins (Chromogranin B and Secretogranin II) and Constitutive Secretory Markers in Rat Pituitary GH4C1 Cells. J Biol Chem 1996; 271: 3575-80.
Jeziorowski T, Watanabe T, Bargsten G, Grube D: Heterogeneity of Pituitary Gonadotrope Cells in Male Rats. Arch Histol Cytol 1997; 60: 355-70.
Rosa P, Basetti M, Weiss U, Huttner WB: Widespread occurrence of Chromogranins/Secretogranins in the matrix of secretory granules of endocrinologically silent pituitary adenomas. J Histochem Cytochem 1992; 40: 523-33.
Nobels FRE, Kwekkeboom DJ, Coopmans W, Schoenmakers CHH, Lindemans J, De Herder WW, Krenning EP, Bouillon R, Lamberts SWJ: Chromogranin A as serum marker for neuroendocrine neoplasia : Comparison with neuron-specific enolase and the subunit of glycoprotein hormones. J Clin Endocrinol Metab 1997; 82: 2622-28.
Colombo P, Siccardi AG, Paganelli G, Magnani P, Songini C, Buffa R, Faglia G, Fazio F: Three-step immunoscintigraphy with anti-chromogranin A monoclonal antibody in tumors of the pituitary region. Eur J Endocrinol 1996; 135: 216-21.
Nobels FRE, Kwekkeboom DJ, Coopmans W, Hoekstra R, De Herder WW, Bouillon R, Lamberts SWJ: A comparison between the diagnostic value of Gonadotropins, -subunit, and chromogranin A and their response to Thyrotropin- releasing hormone in clinically nonfunctioning, -subunit-secreting, and gonadotroph pituitary adenomas. J Clin Endocrinol Metab 1993; 77: 784-9.