
Vol. 38, n.º 3, 2005
REVISTA
ESPAÑOLA DE
Vol. 38, n.º 3, 2005 |
ORIGINALES
Vicente Vicente Ortega1, Antonio Fructuoso Martínez1, M.ª Josefa Yáñez Gascón1, Miguel Alcaraz Baños2, Julián Castillo Sánchez3, Obdulio Benavente-García3, Nuria Álvarez Sánchez4
1 Departamento de Anatomía Patológica.
2 Departamento de Radiología y Medicina Física.
3 Facultad de Medicina, Universidad de Murcia. Furfural
Español, S.A. Murcia.
4 Dercont DELL S.L., Murcia.
vvortega@um.es
RESUMEN
Introducción: La administración de sustancias por vía transdérmica, mediante electroporación por pulsos cortos de alto voltaje, ha experimentado un enorme desarrollo durante la última década. Material y métodos: Aplicamos sobre la piel de cobayas, 5 ml de las suspensiones de tinta china y de hidroxitirosol al 30% en liposomas, aplicando simultáneamente ondas electromagnéticas durante veinte minutos. Realizamos el estudio morfológico-ultraestructural y de análisis de imagen mediante biopsias inmediatas y a las 24 y 96 horas y a los 26 días, así como el estudio cromatográfico por HPLC del hidroxitirosol y sus metabolitos en piel, plasma, músculo e hígado. Resultados: Morfológicamente observamos partículas de tinta china en el estrato córneo y en los queratinocitos epidérmicos en las biopsias inmediatas, mientras que en las posteriores, las observamos además en los anejos y en la dermis papilar y reticular, sin que se observen alteraciones microscópicas ni ultraestructurales. El estudio cromatográfico puso de manifiesto la presencia de hidroxitirosol en todas las muestras analizadas y de algunos de sus metabolitos en hígado y plasma. Conclusión: La electroporación por ondas hectométricas pulsadas ha demostrado el transporte transdérmico de dos sustancias macromoleculares (tinta china e hidroxitirosol) en cobayas.
Palabras clave: vía transdérmica, ultraestructura, electroporación, cobayas.
SUMMARY
Introduction: The transdermal administration of substances via high-voltage short-pulse electroporation has undergone tremendous development over this last decade. Material and Methods: 5 ml of suspension of Indian ink and hydroxytyrosol at 30% in liposomes were applied to the of guinea pigs whilst simultaneously applying electromagnetic waves over a twenty-minute period. A study of the morphological-ultrastructure and image-analysis were performed using biopsies taken at 0, 24 and 96 hours and also at 26 days. A chromatographic study was also carried out via HPLC of the hydroxytyrosol and its metabolites in skin, plasma, muscle and liver. Results: Morphologically speaking, Indian ink particles were observed in the zero hours biopsies at the corneous layer and in epidermal keratinocytes, whilst in subsequent biopsies, said particles were also observed in annexes and in the papillar and reticular dermis with no observed microscopic or ultrastuctural alterations. The chromatographic study revealed the presence of hydroxytyrosol in all samples analysed and several of its metabolites in liver and plasma. Conclusion: Pulsed-hectometric-wave electroporation has demonstrated the transdermal transport of two macromolecular substances, Indian ink and hydroxytyrosol, in guinea pigs.
Key words: transdermal administration, ultrastructural, electroporation, guinea pigs.
INTRODUCCIÓN
La denominada vía transdérmica consiste en la administración de sustancias a través de la piel. Tiene la ventaja de que evita los efectos indeseables de las vías tradicionales (oral, intramuscular y parenteral) pudiendo incluso llegar mediante terapias localizadas a conseguir efectos sistémicos (1,2). Sin embargo, presenta el inconveniente de que solo un pequeño porcentaje de drogas son capaces de atravesar la implacable barrera que representa la piel, además de que dicho tránsito suele ser muy lento (3-5). Se han utilizado distintos métodos físicos y químicos (6), entre estos destaca la iontoforesis que utiliza corrientes eléctricas de bajo voltaje que permiten la ionización de la sustancia y su introducción en la célula por mecanismos de electropulsión, pero ha presentado diversas reacciones adversas (7), entre los segundos destaca la electroporación, que mediante cargas eléctricas u ondas electromagnéticas con pulsos de alto voltaje, es capaz de permitir el paso de sustancias al aumentar la permeabilidad celular con apertura de poros de forma reversible y transitoria (8,9). Más recientemente Denet (10) señala que tales pulsos originarían una perturbación pasajera de la bicapa lipídica de la membrana celular que aumentaría su permeabilidad, aunque no existen evidencias morfológicas del transporte de las sustancias a través de los poros antes citados, basándose hasta ahora solo en evidencias indirectas.
Aunque su uso comenzó con la incorporación del DNA en el interior celular en estudios «in vitro», progresivamente se ha ido utilizando para la transferencia de DNA en estudios «in vivo» y su aplicación a la terapia génica (11,12) así como en la administración de diversos medicamentos (13) tanto en procesos dolorosos (14) como en patologías inflamatorias (15,16); neoplásicas (17,18); vacunas (19-21); etc.
Sin embargo, no hemos encontrado estudios sobre las características morfológicas del transporte transdérmico de las sustancias administradas por este método. Por lo que el objetivo de nuestro trabajo ha consistido en el estudio sistematizado mediante biopsias periódicas de las zonas cutáneas tras la aplicación de un colorante tradicional (tinta china) y el estudio cromatográfico mediante HPLC del compuesto fenólico (hidroxitirosol) y sus metabolitos en piel, sangre, músculo e hígado.
MATERIAL Y MÉTODOS
Animales
Hemos utilizado 10 cobayas de 900-1.200 gramos al inicio del experimento, procedentes de Servicio de Animales de Laboratorio (SACE-Universidad de Murcia, Licencia 30030 2AB) que han sido mantenidos en jaulas individuales con dieta «ad libitum».
Procedimiento experimental
Los animales fueron sedados con 0,3 ml/i.m. de clorhidrato de ketamina (Merial S.A., Lyon, Francia) y a continuación se les rasuró una zona de la piel del lomo de 6 ´ 3 cm, que fue lavada con jabón neutro y secada.
A tres animales les administramos, mediante goteo, 5 ml de la suspensión de tinta china (Royal Talem, Holanda, compuesta por partículas de carbón micronizado, goma adherente, sulfato de hierro y grasa) al 5% en liposomas de lecitina de soja. Simultáneamente deslizamos el cabezal emisor de ondas electromagnéticas de alta frecuencia (ondas hectométricas sinusoidales moduladas y pulsadas) emitidas por el aparato TDES (Dercont Dell®, Murcia, España) durante veinte minutos. Tras lo cual se procedió al lavado de la zona con jabón neutro y secado.
A tres animales les aplicamos 2 ml de la suspensión de hidroxitirosol (Furfural Español S. A., Murcia, España) al 30% (0,6 g) en liposomas de lecitina de soja de modo similar que en el grupo anterior.
Los cuatro animales restantes fueron utilizados como controles:
A dos animales le aplicamos la tinta china del modo similar al grupo anterior tratado con ella, pero sin administrar las ondas electromagnéticas, es decir aplicando el cabezal emisor pero con el aparato desconectado de la red eléctrica.
A dos animales le aplicamos 5 ml de lecitina de soja pero sin tinta china, y aplicamos las ondas como en el primer grupo de tratamiento.
Método anatomopatológico
Para el estudio microscópico realizamos biopsias punch de 8 mm de las zonas cutáneas tratadas con tinta china y a los dos controles correspondientes, inmediatamente después del tratamiento y a las 24 h, 96 h y al mes del tratamiento.
Para el estudio microscópico óptico las muestras cutáneas obtenidas fueron fijadas en formol neutro tamponado al 10% y procesadas por el método habitual para su inclusión en parafina. Realizamos secciones seriadas de 4 µm, que se tiñeron con Hematoxilina-Eosina.
Para el estudio al microscópico electrónico de transmisión, muestras cutáneas representativas de 1 mm3 fueron fijadas en formaldehído/glutaraldehido (22), postfijados con tetróxido de osmio al 1%, teñidas con acetato de uranilo al 1,5%, deshidratadas con alcoholes a concentraciones crecientes e impregnadas con resinas epoxy. Las secciones ultrafinas fueron estudiadas y fotografiadas en un microscopio electrónico ZEISS EM 10C.
Observación de las partículas de tinta china mediante microscopía electrónica
Diluciones de tinta china al 2,5 y 5% en agua destilada fueron incluidas en agar. Los bloques de agar se procesaron por el método habitual para microscopía electrónica de transmisión (SACE, Universidad de Murcia). Las secciones ultrafinas fueron estudiadas y fotografiadas en un microscopio electrónico ZEISS EM 10C.
Para el estudio con el microscopio electrónico de barrido, la tinta china fue diluida al 5 y 10% en agua destilada. Se realizaron extensiones de las muestras sobre cubreobjetos, se dejaron secar y se recubrieron con una capa de oro (SEM Coating System) de unos 200 Å de espesor en un vaporizador Bio-Rad. La observación se realizó en un microscopio electrónico Jeol 6.100, capturando la imagen digital mediante el detector Link-Isis
Estudio cromatográfico
A las dos horas y media del tratamiento se realizó el análisis del contenido del hidroxitirosol en las muestras tisulares (piel, músculo e hígado) y en sangre, utilizando para ello un método de HPLC. Los tejidos fueron homogeneizados (Polytron CH-610, Kriens-Luzen, Suiza) utilizando una mezcla metanol/agua (50/50). Alícuotas del homogeneizado y la sangre fueron centrifugados a 1000 xg durante 5 minutos. Los sobrenadantes fueron filtrados a través de una membrana de nylon de 0,45 µm. Las muestras fueron congeladas a -80 ºC hasta su análisis.
Se ha utilizado un equipo Hewlett-Packard HP 1100 con detector array de diodos. La fase estacionaria fue una columna analítica LiChrospher 100 (Merck) (250 ´ 4 mm i.d., 5 µm) termostatizada a 30ºC, el flujo fue de 1 ml/mn y el eluido monitorizado a 280 nm. La fase móvil fue acético 2,5% (A) y acetonitrilo (B), con el siguiente gradiente: las condiciones iniciales (95% A) pasaron a 50% A en cuarenta minutos y posteriormente a 20% A en diez minutos, volviendo a las condiciones iniciales en diez minutos.
El hidroxitirosol se identificó por comparación de su tiempo de retención con el correspondiente estándar cromatográfico (99% de pureza) y su contenido medido por comparación del área del pico frente al estándar.
Análisis de imagen
Para la valoración de la distancia entre los espacios intercelulares o canales y el diámetro de las partículas de tinta china se utilizó un equipo de análisis de imagen mediante el software MIP4.5 (Microm Image Processing software, Consulting Image Digital, Barcelona, España), previa digitalización y calibración de las imágenes de microscopía electrónica para obtener medidas reales en micrómetros.
Se trazaron 8 medidas de distancia por canal o espacio intercelular, obteniéndose un valor medio representativo de todas las medidas. Para la valoración de las partículas de tinta china, la imagen digitalizada fue segmentada por niveles de gris, ajustándose a las partículas. Para cada partícula se valoró el diámetro máximo, el diámetro equivalente y el volumen equivalente en un total de 500 partículas.
RESULTADOS
Estudio morfológico-ultraestructural
En los tres animales a los que se les administró la tinta china y las ondas electromagnéticas, el estudio microscópico-óptico, de las biopsias realizadas inmediatamente tras su aplicación, demostró la presencia de partículas de pigmento negro brillante, que se disponían en múltiples acúmulos pequeños sobre la superficie del estrato córneo, entre las láminas córneas así como en los queratinocitos de la epidermis y los poros foliculares; aunque no las observamos en los queratinocitos de la porción intradérmica de los folículos pilosos ni tampoco en la dermis (fig. 1); mientras que en las restantes biopsias realizadas a las 24 y 96 horas y a los 26 días de la administración de la tinta china, observamos las partículas de tinta en las localizaciones anteriores (estrato córneo y queratinocitos epidérmicos), y también se localizaban en los queratinocitos de las porciones intradérmicas de los folículos pilosos, así como en la dermis, tanto en la papilar como en la reticular, en el interior del citoplasma de los macrófagos, preferentemente localizados alrededor de los vasos sanguíneos y también de forma individualizada entre los haces de fibras colágenas y músculos (fig. 2).
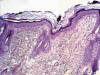
Fig. 1: Partículas
de tinta china en las biopsias después del tratamiento. H.E. 312,5x.
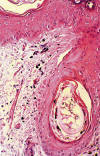
Fig. 2: Biopsia
después de 24 horas del tratamiento. Detalle del epitelio en los queratinocitos
epidérmicos y foliculares y en la dermis. H.E. 500x.
El estudio microscópico electrónico demostró la presencia de las partículas en el citoplasma de los queratinocitos, como partículas de morfología poligonal con los bordes poco angulares, mal delimitados, y de mayor electrodensidad que los gránulos de queratohialina (fig. 3). Las múltiples secciones semifinas seriadas (fig. 4) nos permitieron visualizar, en las secciones ultrafinas seleccionadas, las distintas fases del transporte de las partículas de tinta china desde los queratinocitos foliculares hasta la dermis, que en algunas zonas consistía en la apertura de canales o «poros» por separación total de las estructuras desmosómicas entre las dos células adyacentes, cuyos diámetros máximos oscilaban entre 0,84 µm-3,10 µm (media de 2,01 µm±0,58), que permitían el paso directo de las partículas a la dermis (fig. 5), mientras que en otras zonas observamos la apertura parcial de dichos espacios intercelulares, que afectaba en unas áreas, a la porción interna de la unión entre las células adyacentes formando un espacio intercelular parcial que contenía varias partículas (fig. 6), que en las secciones ultrafinas siguientes, dicha separación intercelular llevaba a la formación de «poros» o espacios en la porción central de la unión de las células vecinas (fig. 7), y en las secciones siguientes del «poro» afectaba ya a las porciones externas de dicha unión intercelular con comunicación con la dermis adyacente (fig. 8). A veces se observaba la formación de varios espacios intercelulares intercomunicados entre sí con varias partículas de pigmento de distintos tamaños, que desde la médula del pelo salían al espacio intercelular de la dermis. El tamaño de las partículas observadas en los espacios intercelulares oscilaban entre 0,047 y 3,097 µm, con una media de 0,276 µm.
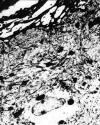
Fig. 3: Sección
ultrafina con partículas de tinta china en el estrato córneo y en queratinocitos
epidérmicos. 3150x.

Fig. 4: Sección
semifina de folículo piloso después de 24 horas con apertura de los espacios
intercelulares o «poros». Azul de toluidina 400x.
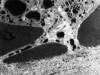
Fig. 5: Apertura
intercelular (poro) con varias partículas de tinta china que comunica el
interior del folículo piloso con la dermis 12.500x.
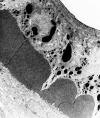
Fig. 6: Apertura
parcial del espacio intercelular en el folículo piloso 8.500x.
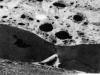
Fig. 7: Apertura
parcial del espacio intercelular en el folículo piloso con formación de espacio
intercelular y con partículas de tinta china en su interior 10.000x.

Fig. 8: Apertura
parcial del espacio intercelular en el folículo piloso en la porción externa del
folículo piloso 8.500x.
Asimismo, observamos acúmulos de dichas partículas tanto en la dermis papilar como reticular, localizadas entre los haces de fibras colágenas, en la proximidad de las glándulas sebáceas, músculos y vasos sanguíneos, en donde solían mostrar configuración poligonal con bordes afilados, así como en el interior de los citoplasmas de los macrófagos. Sus tamaños oscilaban entre 0,28 µm y 1,60 µm con un valor medio de 0,82 µm.
En el estudio microscópico electrónico de barrido y transmisión (figs. 9a y b) realizado directamente a partir de la suspensión de la tinta china, las partículas de tinta mostraban morfología poligonal y esférica respectivamente, de forma individual o en acúmulos. En el 80% de las partículas analizadas sus tamaños oscilaban entre 0,25 µm y 0,06 µm con un valor medio de 0,15 µm.

Fig. 9: Partículas
de tinta china en suspensión. MEB (22.000x) y MET (24.000x).
Las zonas cutáneas controles en las que aplicamos exclusivamente la suspensión de tinta china, sin que aplicáramos las ondas electromagnéticas, mostraban partículas de pigmento similares a las descritas anteriormente, tanto al microscopio óptico como electrónico, pero localizadas exclusivamente en el estrato córneo; mientras que en los animales a los que solo administramos las ondas sin aplicar tinta china no presentaban partículas de pigmento.
Un hecho que debemos destacar correspondía a que en ninguna de las muestras cutáneas tratadas y en las controles, observamos alteraciones tisulares microscópicas ni las más sutiles a nivel ultraestructural, tanto a nivel del epitelio como en los anejos cutáneos ni en la dermis, que son características de la injuria celular como tumefacción y vacuolización celular, nuclear o de los orgánulos, alteraciones de las membranas, de las mitocondrias, necrosis, etc.
Análisis cromatográfico
El análisis por HPLC de las muestras de piel demostró la presencia del hidroxitirosol sin metabolitos, con una concentración de 700 mg/Kg de tejido (4,49 mM). En el músculo apareció un perfil similar al anterior, aunque con una concentración menor de 235 mg/Kg de tejido (1,51 mM). En las muestras hepáticas observamos además el pico correspondiente al hidroxitirosol y los de casi todos sus metabolitos (sulfatos y glucurónidos). La concentración de hidroxitirosol libre en el tejido hepático fue de 24,7 mg/kg de tejido (0,158 mM). Por último, en el plasma también se detectó hidroxitirosol libre y algunos de sus metabolitos, siendo la concentración de hidroxitirosol libre de 0,017 mM.
DISCUSIÓN
La electroporación, con una historia de mas de treinta años (23), constituye un método físico que utiliza pulsos cortos de alto voltaje para hacer permeable la membrana celular a los iones (24), anticuerpos, RNA (25) y DNA, drogas, etc., y fue utilizada en principio para la transferencia de genes a células de ratón (26). Durante la década de los ochenta se desarrolló la administración de macromoléculas a células eucariotas in vitro (24) y a partir de los noventa se utilizó en la administración de principios activos por vía transdérmica (27-29), correspondiendo a Belehrader (31) el primer estudio clínico sobre el uso de la electroporación en la quimioterapia de tumores, que fue seguido de múltiples trabajos que la desarrollaron: Heller (32), Mir (33), Gehl (4), Sersa (35), etc. El paso de las sustancias se ha relacionado con la formación de poros en la membrana celular tras la aplicación de los pulsos eléctricos (36,37) a nivel de la capa lipídica de la membrana celular e incluso a través del estrato córneo (29). Otros estudios han mostrado la evidencia indirecta de que pulsos de alto voltaje causan cambios en la estructura de la piel (38,39) y posiblemente llevan a la formación de caminos acuosos durante la aplicación del pulso eléctrico. Sin embargo, el mecanismo íntimo de tales fenómenos no está claramente demostrado, ya que los «poros» no han sido evidenciados con ninguna técnica microscópica, posiblemente debido a su pequeño tamaño y a su carácter transitorio y reversible (40).
El mecanismo del paso de sustancias a través de la piel ha sido explicado por dos rutas; transcelular e intercelular, tanto a través de la epidermis como por vía transfolicular (6) y relacionados con los distintos tipos de pulsos utilizados (10,40,41), de modo que cuando se aplican pulsos cortos de alto voltaje el transporte se realizaría fundamentalmente por vía transcelular; mientras que cuando se disminuye el voltaje o se aumenta la duración del pulso el transporte ocurre preferentemente de modo intercelular o transfolicular (42,43). En estudios previos se ha descrito el paso de partículas de 0,2; 4 e incluso 45 µm en la piel de ratones «hairless» con pulsos de 120 V y de 1,2 ms (44).
Sin embargo, en nuestro trabajo, utilizando exclusivamente pulsos cortos de alto voltaje observamos los dos mecanismos descritos de transporte, transcelular e intercelular, ya que en nuestro estudio morfológico-ultraestructural sistematizado observamos la presencia de partículas de tinta china tanto en el estrato córneo, entre las láminas córneas, en los poros foliculares como en los citoplasmas de lo queratinocitos en todas las capas de la epidermis y en la dermis papilar, lo que indica el paso transcelular hasta la dermis, pero también observamos dicho paso de forma detallada a través de los espacios intercelulares de los queratinocitos adyacentes en los folículos pilosos y la llegada de las partículas de tinta china a la dermis. Sin que hayamos precisado utilizar sustancias queratolíticas como la urea o tiosulfato sódico, como han descrito previamente Ilic (45) para hacer pasar las sustancias a través del estrato córneo.
También el estudio cromatográfico ha demostrado el paso de la otra macromolécula administrada, el hidroxitirosol (compuesto fenólico abundante en el aceite de oliva que pertenece al grupo de antioxidantes naturales y que ha demostrado propiedades frente a la formación de radicales libres, acción antiinflamatoria, etc) tanto a la sangre como a los tejidos estudiados (piel, músculo e hígado).
También diversos estudios previos habían descrito la posible formación de «macroporos» de las membranas celulares tras la aplicación de corrientes de voltaje medio (46,47) así como que la formación de estos «poros» sería de distribución irregular en la superficie córnea (39), e incluso se ha señalado que el paso de sustancias a través de los «poros» sería distinto, siendo máximo por la porción central de los «poros», mientras que alrededor presentarían mayor resistencia al paso, permitiendo solo el transporte de iones de pequeño tamaño (48). Sin embargo, nuestro estudio parece demostrar que los espacios intercelulares creados por la aplicación de los pulsos adaptan su diámetro al tamaño de las partículas que lo atraviesan como demuestran las imágenes seriadas y por el análisis de imagen realizado.
Una vez que las partículas de tinta se encuentran en la dermis tienden a localizarse, como en el caso de los tatuajes, en el citoplasma de los macrófagos, en la vecindad de los anexos cutáneos y músculo así como entre los haces de las fibras colágenas.
Un aspecto muy importante de su utilización clínica corresponde s los posibles efectos sobre la piel y tejidos circundantes, para lo que se han desarrollado diverso métodos para establecer la tolerancia de la piel a dichos pulsos eléctricos como: estudio macroscópico mediante examen directo, medida de las propiedades eléctricas de la piel, métodos de bioingeniería no invasivos, estudios ultraestructurales, etc. (10). No obstante, las alteraciones descritas tras la aplicación de pulsos de alto voltaje suelen ser moderadas y reversibles, entre las que destacarían: la sensación dolorosa por excitación de los nervios y músculos próximos, prurito, sensación de quemazón y/o pinchazo, eritema y disminución de la resistencia eléctrica de la piel tratada, etc. (29,49-53). En nuestro estudio, no hemos medido la sensación de dolor, prurito, pinchazos, etc. ni la resistencia eléctrica de la piel. Habiendo observado solo el eritema, que era de grado leve y pasajero, pues desaparecía en pocas horas. No obstante, si podemos afirmar que la aplicación de pulsos cortos de alto voltaje sobre la piel del cobaya, durante veinte minutos, no originó alteraciones titulares ni siquiera las mas sutiles a nivel ultraestructural como la tumefacción y vacuolización citoplasmática o de los orgánulos, irregularidad de las membrana celulares, nucleares y de los orgánulos, alteraciones de los componentes nucleares con desorganización granulo-fibrilar, etc. que han sido descritas como características de la injuria celular por diversos agentes (54).
Asimismo, nuestro estudio ha demostrado la idoneidad del cobaya como modelo animal en este tipo de estudios, por ser un animal dócil, de fácil manejo en el laboratorio (anestesia, biopsias, cicatrización, etc.) y por presentar, junto con el cerdo, las características cutáneas más similares a las de la piel humana como ha sido descrito previamente por Panchangnula (15).
En conclusión, nuestro estudio demuestra la eficacia de la electroporación mediante pulsos cortos de alto voltaje en la administración transdérmica de dos macromoléculas: un colorante tradicional (tinta china) y un compuesto fenólico (hidroxitirosol); que puede constituir una prometedora alternativa no invasiva para la administración transdérmica de otros principios activos.
Agradecimientos
Agradecemos a Víctor Bolarín Lucas, técnico en Anatomía Patológica por su asistencia técnica, a Nuria Álvarez (alumna de tercer ciclo) y a Enrique Bautista y Fran Zapata del Servicio de Animales de Laboratorio (SACE) de la Universidad de Murcia. Este trabajo ha sido parcialmente financiado con una ayuda del Plan de Ciencia y Tecnología de la Región de Murcia (Ref. 2I04SU012).
BIBLIOGRAFÍA
Prausnitz MR. The effects of current applied to the skin: a review for transdermal drug delivery. Adv Drug Deliv Rev. 1996a; 18: 395-425.
Shin SC, Cho CW, Choi HK. Permeation of piroxicam from the poloxamer gels. Drug Dev Ind Pharm 1999; 25: 273-78.
Guy RH. Current status and future prospects of transdermal drug delivery. Pharm Res 1996; 13: 1765-9.
Foldvari M. Non-invasive administration of drugs through the skin: challenges in delivery system design. Pharm Sci Technol Today 2000; 3: 417-25.
Naik A, Kalia YN, Guy RH. Transdermal drug delivery: overcoming the skin’s barrier function. Pharm Sci Technol Today 2000; 3: 318-26.
Banga AK, Prausnitz MR. Assessing the potential of skin electroporation for the delivery of protein- and gene-based drugs. Trends Biotechnol 1998; 16: 408-12.
Jadoul A, Bouwstra J, Preat V. Effects of iontophoresis and electroporation on stratum corneum-review of the biophysical studies. Ddv Drug Deliv Rev 1999; 35: 89-105.
Rols MP, Teissie J. Electropermeabilization of mammalian cells to macromolecules: control by pulse duration. Biophys J 1998; 75: 1415-23.
Neumann E, Kakorin S. Digression on membrane electroporation for drug and gene delivery. Technol Cancer Res Treat 2002; 1: 329-40.
Denet AR, Vanbever R, Preat V. Skin electrooporation for transdermal and topical delivery. Adv Drug Deliv Rev 2004; 56: 659-74.
Dean DA. Electroporation of the vasculature and the lung. DNA Cell Biol. 2003; 22: 797-806.
Li S, Xia X, Mellieon FM, Liu J, Steele S. Candidate genes associated with tumor regression mediated by intratumoral IL-12 electroporation gene therapy. Mol Ther 2004; 9: 347-54.
Mori K, Hasegawa T, Sato S, Sugibayashi K. Effect of electric field on the enhanced skin permeation of drugs by electroporation. J Control Release 2003; 90: 171-9.
Lan CY, Tan PH, Cheng JT, Lu HF, Lin MW, Hsiao PN et al. Immunoneutralization of c-Fos using intrathecal antibody electroporation attenuates chronic constrictive injury-induced hyperalgesia and regulates prepodynorphin expression in rats. Anesthesiology 2003; 99: 938-46.
Panchagnula, R. Transdermal delivery of drugs. Ind J Pharmacol 1997; 29: 140-56.
Badkar AV, Betagen GV, Hofmann GA, Banga AK. Enhancement of transdermal iontophoretic delivery of a liposomal formulation of colchicines by electroporation. Drug Deliv 1999; 6: 111-5.
Hyacinthe M, Jaroszeski MJ, Dang VV, Coppola D, Karl RC, Gilbert RA et al. Electrically enhanced drug delivery for the treatment of soft tissue sarcoma. Cancer 1999; 85: 409-17.
Jaroszeski MJ, Dang V, Pottinger C, Hickey J, Gilbert R, Heller R. Toxicity of anticancer agents mediated by electroporation in vitro. Anticancer Drugs 2000; 11: 201-8.
Li S, Benninger M. Applications of muscle electroporation gene therapy. Curr Gene Ther 2002; 2: 101-5.
Dayball K, Millar J, Miller M, Wan YH, Bramson J. Electroporation enables plasmid vaccines to elicit CD8+ T cell responses in the absence of CD4+ T cells. J Immunol 2003; 171: 3379-84.
Davalos RV, Otten DM, Mir LM, Rubinsky B. Electrical impedance tomography for imaging tissue electroporation. IEEE Trans Biomed Eng 2004; 51: 761-7.
Karnovsky MJ. A fomaldehyde-glutaraldehyde fixative of high osmolarity for use in electrón microscopy. J Cell Biol 1965; 27: 137-8.
Tsong TY. Electroporation of cell membranes. Biophys J 1991; 60: 297-306.
Mir LM, Banoun H, Paoletti C. Introduction of definite amounts of nonpermeant molecules into living cells after electropermeabilization: direct access to the cytosol. Exp Cell Res 1988; 175: 15-25.
Teruel MN, Blanpied TA, Shen K, Augustine GJ, Meyer T. A versatile microporation technique for the transfection of cultured CNS neurons. Neurosci Methods 1999; 93: 37-48.
Neumann E, Schaefer-Ridder M, Wang Y, Hofschneider PH. Gene transfer into mouse lyoma cells by electroporation in high electric fields. EMBO J 1982; 1: 841-5.
Belehradek J Jr, Orlowski S, Poddevin B, Paoletti C, Mir LM. Electrochemotherapy of spontaneous mammary tumours in mice. Eur J Cancer 1991; 27: 73-6.
Mir LM, Orlowski S, Belehradek J Jr, Paoletti C. Electrochemotherapy potentiation of antitumour effect of bleomycin by local electric pulses. Eur J Cancer 1991; 27: 68-72.
Prausnitz MR, Bose VG, Langer R, Weaver JC. Electroporation of mammalian skin: a mechanism to enhance transdermal drug delivery. Proc Natl Acad Sci U S A 1993; 90: 10504-8.
Salford LG, Persson BR, Brun A, Ceberg CP, Kongstad PC, Mir LM. A new brain tumour therapy combining bleomycin with in vivo electropermeabilization. Biochem Biophys Res Commun. 1993; 194: 938-43.
Belehradek M, Domenge C, Luboinski B, Orlowski S, Belehradek J Jr, Mir LM. Electrochemotherapy, a new antitumor treatment. First clinical phase I-II trial. Cancer 1993; 72: 3694-700.
Heller R, Jaroszeski MJ, Glass LF, Messina JL, Rapaport DP, DeConti RC et al. Phase I/II trial for the treatment of cutaneous and subcutaneous tumors using electrochemotherapy. Cancer 1996; 77: 964-971.
Mir LM, Glass LF, Sersa G, Teissie J, Domenge C, Miklavcic D et al. Effective treatment of cutaneous and subcutaneous malignant tumours by electrochemotherapy. Br J Cancer. 1998; 77: 2336-42.
Gehl J, Geertsen PF. Efficient palliation of haemorrhaging malignant melanoma skin metastases by electrochemotherapy. Melanoma Res 2000; 10: 585-9.
Sersa G, Stabuc B, Cemazar M, Miklavcic D, Rudolf Z. Electrochemotherapy with cisplatin: the systemic antitumour effectiveness of cisplatin can be potentiated locally by the application of electric pulses in the treatment of malignant melanoma skin metastases. Melanoma Res 2000; 10: 381-5.
Treco DA, Selden RF. Non-viral gene therapy. Mol Med Today 1995; 1: 314-21.
Weaver JC. Electroporation theory: concepts and mechanisms. En: Nickoloff JA, ed. Molecular Biology: Methods. Totowa: Human Press; 1995: 3-28.
Edwards D.A. Prausnitz M.R. Langer R., Weaver J.C. Analysis of enhanced transdermal transport by skin electroporation. J Control Release 1995; 34: 211-21.
Prausnitz MR, Gimm JA, Guy RH, Langer R, Weaver JC, Cullander C. Imaging regions of transport across human stratum corneum during high-voltage and low-voltage exposures. J Pharm Sci 1996b; 85: 1363-70.
Banga AK, Bose S, Ghosh TK. Iontophoresis and electroporation: comparisons and contrasts. Int J Pharm 1999; 179:1-19.
Pliquett UF, Zewert TE, Chen T, Langer R, Weaver JC. Imaging of fluorescent molecule and small ion transport through human stratum corneum during high voltage pulsing: localized transport regions are involved. Biophys Chem 1996; 58: 185-204.
Pliquett UF, Vanbever R, Preat V, Weaver JC. Local transport regions in human stratum corneum due to short and long high- voltage pulses. Bioelectrochem Bioenerg 1998; 47: 151-61.
Vanbever R, Preat V. In vivo efficacy and safety of skin electroporation. Adv Drug Deliv Rev 1999 Jan 4; 35: 77-88.
Hoffmann GA, Rustrum WV, Suder KS. Electro-incorporation of microcarriers as a method for the trnasdermal delivery of large molecules. Bioelectrochem Bioeneerg 1995; 38: 209-222.
Ilic L, Gowrishankar TR, Vaughan TE, Herndon TO, Weaver JC. Spatially constrained skin electroporation with sodium thiosulfate and urea creates transdermal microconduits J Control Release 1999; 61: 185-202.
Chizmadzhev YA, Indenbom AV, Kuzmin PI, Galichenko SV, Weaver JC, Potts RO. Electrical properties of skin at moderate voltages: contribution of appendageal macropores. Biophys J 1998a; 74(2 Pt 1): 843-56.
Chizmadzhev YA, Kuzmin PI, Weaver JC, Potts RO. Skin appendageal macropores as a possible pathway for electrical current. J Investig Dermatol Symp Proc. 1998; 3: 148-52.
Pliquett UF, Vanbever R, Preat V, Weaver JC. Local transport regions in human stratum corneum due to short and long high- voltage pulses. Bioelectrochem Bioenerg 1998; 47: 151-61.
Pliquett UF, Langer JC, Weaver JC. Changes in the passive electrical properties of human stratum corneum due to electroporation. Biochem Biophys Acta 1995; 1239: 111-21.
Riviere JE, Monteiro-Rivière NA, Rogers RA, Bommannan D, Tamada JA, Potts RO. Pulsatile transdermal delivery of LHRH using electroporation: Drug delivery and skin toxicology. J Control Release 1995; 36: 229-33.
Jadoul A, Tanajo H, Preat V, Spies F, Boddé H. Electroperturbation of human stratum corneum fine structure by high voltage pulses: a freeze fracture electron microscopy and differential thermal analysis study. J Invest Dermatol Symp Proc 1998; 3: 153-8.
Vanbever R, Leroy MA, Preat V. Transdermal permeation of neutral molecules by electroporation. J Control Release 1998; 54: 243-50.
Dujardin N, Staes E, Kalia Y, Clarys P, Guy R, Preat V. In vivo assessment of skin electroporation using square wave pulses. J Contol Release 2002; 79: 219-27.
Rubin E, Gorstein F, Schwarting R, Strayer DS. Cell injury. In: Strayer D, ed. Rubin’s Pathology. Philadelphia: Lippincott Williams and Wilkins; 2005: 3-39.