
Vol. 39, n.º 3, 2006
REVISTA
ESPAÑOLA DE
Vol. 39, n.º 3, 2006 |
CASUÍSTICA
Lidia Atienza Cuevas, M.ª José Añón Requena, Rosario Guerrero Cauqui, Manuel Beltrán Ruiz-Henestrosa, José Pérez Requena
Servicio de Anatomía Patológica del Hospital
Universitario Puerta del Mar. Cádiz.
lidia_atienza@ono.com
RESUMEN
Introducción: El gliosarcoma es una variante rara de glioblastoma que se caracteriza por un patrón bifásico en el que alternan áreas de diferenciación glial y mesenquimal. La presencia de alteraciones genéticas idénticas en los componentes glial y sarcomatoso apoya la idea de un origen monoclonal del gliosarcoma. Pacientes y métodos: Presentamos un caso de gliosarcoma con diferenciación adenoide y fibras de Rosenthal. Conclusiones: La existencia de fibras de Rosenthal es un hallazgo muy poco habitual en el seno de tumoraciones gliales de alto grado.
Palabras clave: gliosarcoma, glioblastoma, sarcoma, tumores cerebrales, carcinoma.
SUMMARY
Introduction: Gliosarcoma is a rare glioblastoma variant characterized by a biphasic tissue pattern with alternating areas displaying glial and mesenchymal differentiation. The presence of identical genetic alterations in both gliomatous and sarcomatous components strongly supports the concept of a monoclonal origin of gliosarcoma. Patients and methods: We report a case of gliosarcoma with adenoid differentiation and Rosenthal fibers. Conclusions: The presence of Rosenthal fibers is a very uncommon finding in high grade glial neoplasms.
Key words: gliosarcoma, glioblastoma, sarcoma, cerebral tumors, carcinoma.
INTRODUCCIÓN
El Gliosarcoma es una variante del Glioblastoma (Grado IV de la OMS) que se caracteriza histológicamente por un patrón bifásico con áreas tumorales de diferenciación glial y mesenquimal y que se localiza, con mayor frecuencia, en los lóbulos temporal y frontal, siendo más frecuente en varones (1). Las áreas gliales suelen corresponder habitualmente a un glioblastoma y presenta, en muy raras ocasiones, zonas de diferenciación escamosa o glandular con patrones trabecular, adenoide e incluso formando estructuras papilares debiéndose hacer el diagnóstico diferencial con metástasis de carcinoma (2,3,5). Las áreas sarcomatosas suelen corresponder, preferentemente, a fibrosarcoma o histiocitoma fibroso maligno aunque, ocasionalmente, puede apreciarse diferenciación muscular, ósea o cartilaginosa (3,4).
DESCRIPCIÓN DEL CASO
Varón de 67 años sin antecedentes personales de interés que inicia un mes antes de su ingreso un cuadro de cefalea frontooccipital de intensidad creciente, que no cede con analgésicos así como pérdida de memoria para hechos recientes. En la exploración física se aprecia buen estado general, sin déficit sensitivo ni motor, apreciándose en la exploración clínica del campo visual cuadrantanopsia superior. El hemograma, la bioquímica, la coagulación y los marcadores tumorales se encuentran dentro de los límites de la normalidad. En el TAC craneal se aprecia una lesión ocupante de espacio de 6cm de diámetro máximo en el lóbulo temporal izquierdo, con edema perilesional y ligero desplazamiento de la línea media. En la RM se observa en dicha lesión zonas necróticas en su interior y edema perilesional sugestivo de glioma de alto grado (fig. 1). El paciente es intervenido quirúrgicamente mediante una craneotomía temporal izquierda, procediéndose a la exéresis de la lesión.
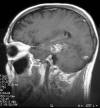
Fig. 1:
Imagen de la RMN craneal que muestra una lesión ocupante de espacio en el lóbulo
temporal izquierdo posterior.
Se remitieron para estudio anatomopatológico dos fragmentos de coloración blanquecinoparduzca con áreas amarillentas de 1,5 y 4 cm.
El estudio microscópico mostró una densa y amplia proliferación tumoral de patrón bifásico con un componente glial constituido por células gemistocíticas y pleomórficas, con alto índice mitótico alternando con proliferación endoteliovascular, vasos trombosados, áreas de necrosis, presencia de frecuentes fibras de Rosenthal (fig. 2) y focos de células epitelioides (fig. 3) adoptando arquitectura adenoide junto a un denso y amplio componente sarcomatoso constituido por células fusiformes y pleomórficas, con alto índice mitótico y alta densidad de trama reticulínica. Las técnicas de inmunohistoquímica mostraron positividad intensa para Proteína Gliofibrilar Ácida (PGFA) (fig. 4) y para citoqueratina de amplio espectro (AE1/AE3) (fig. 5) en los elementos gliales y en las fibras de Rosenthal, positividad débil para citoqueratina de bajo peso (CK8) en las células del componente glial y en las áreas adenoides y positividad intensa para Vimentina en el componente sarcomatoso sin nítida delimitación con el componente glial.
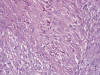
Fig. 2:
Detalle del gliosarcoma con abundantes fibras de Rosenthal en las áreas gliales.
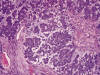
Fig. 3:
Detalle del gliosarcoma con los focos de diferenciación adenoide.
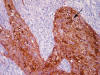
Fig. 4:
Positividad intensa para PGFA en las áreas gliales y las fibras de Rosenthal
(flecha).
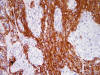
Fig. 5:
Positividad intensa para Citoqueratina de amplio espectro (AE1/AE3) en las áreas
gliales.
Con estos resultados el diagnóstico emitido fue de Gliosarcoma (Grado IV de la OMS).
DISCUSIÓN
El término gliosarcoma fue acuñado por Stroebe en 1898 y representa aproximadamente el 2% de los glioblastomas (1). En 1958 Feigin y Gross definieron el gliosarcoma como un subtipo de glioblastoma, en el que la proliferación vascular había adquirido características sarcomatosas (6) considerando que el punto de partida de dicha proliferación pudiera proceder del entorno vascular: células endoteliales, pericitos, células musculares lisas o histiocitos. Otras hipótesis se apoyan en la capacidad oncogénica del tumor glial, que induciría la transformación sarcomatosa del tejido conjuntivo adyacente (7). Considerando esta posibilidad tendríamos, en sentido contrario, al sarcoglioma, en el que un sarcoma induciría la transformación tumoral del componente glial vecino (8). Recientes estudios genéticos han demostrado un origen único (glial) de ambos componentes tumorales encontrándose en dos casos idénticas mutaciones del PTEN en los componentes glial y sarcomatoso. Estas muestras presentaban delección del p16, idéntica mutación del p53, o coamplificación de mdm2 y CDK4 en ambas áreas tumorales. La presencia de idénticas alteraciones genéticas en ambos componentes gliomatoso y sarcomatoso apoyan manifiestamente un origen único del gliosarcoma (9).
Asimismo, en el caso que presentamos, en el seno de las áreas gliomatosas, se observan frecuentes fibras de Rosenthal que supone un hallazgo muy poco habitual en el seno de tumoraciones gliales de alto grado (10,11) así como focos tumorales de diferenciación adenoide. Se conoce, al respecto, muy poco de la genética molecular de los elementos epiteliales vistos en el gliosarcoma o glioblastoma. Rubinstein propuso una hipótesis patogénica por la cual los astrocitos neoplásicos podrían adquirir características epiteliales, planteando que podría ser debido a un mecanismo de presión de los astrocitos neoplásicos sobre la porción sarcomatosa (7). Kepes y cols. expusieron que la explicación de Rubinstein no era satisfactoria, ya que las características adenoides existentes en el contexto de un glioblastoma multiforme o astrocitoma anaplásico podrían deberse a una doble diferenciación de los astrocitos neoplásicos (2). En este sentido, Ozoleck y cols. hallaron similares alteraciones genéticas en ambos componentes (glial y epitelial) con pérdida de alelos en los cromosomas 1p, 9p 10q, 17p y 19q, apoyando el origen único de ambos componentes. La presencia de focos de diferenciación epitelial, en relación con el componente glial, aún siendo muy poco frecuente en el seno de un gliosarcoma, debemos tenerla en cuenta para no confundirla con metástasis de carcinoma (12,13). Otros tumores primarios del SNC pueden simular metástasis de carcinoma, como el papiloma de los plexos coroideos, el ependimoma mixopapilar, el adenoma hipofisario, el meningioma papilar, los meduloblastomas y entre los gliomas aquellos que pueden presentar diferenciación epitelial: el glioblastoma, el gliosarcoma y el astrocitoma anaplásico (2).
Respecto al pronóstico, se ha sugerido que los gliosarcomas tienen una evolución algo más favorable que los glioblastomas multiformes, pero grandes ensayos clínicos no han mostrado diferencias significativas en ese sentido (14).
AGRADECIMIENTOS
A Don José María Gómez Pérez, por su colaboración en el montaje técnico y fotográfico de este artículo.
BIBLIOGRAFÍA
Kleihues P, Webster KC, editores. Tumours of the Nervous System. Pathology and genetics. World Health Organization Classification of Tumours. Lyon: IARC. 2000. p. 42-4.
Kepes JJ, Fulling KH, Garcia JH. The clinical significance of «adenoid» formations of neoplastic astrocytes, imitating metastatic carcinoma, in gliosarcomas. A review of five cases. Clin Neuropathol 1982; 1: 139-50.
Kim DS, kang SK., Chi JG. Gliosarcoma: A case with unusual epithelial feaure. J Korean Med Sci 1999; 14: 345-50.
Alameda F, Corominas JM, Galitó E, Guardiola MJ, Serrano, S. Gliosarcoma con diferenciación osteoblástica y condroblástica. Patología 1996; 29: 345-7.
Kato K, Watanabe M. Glioblastoma multiforme with epithelial appearance: a case report. Brain Tumor Pathol 1999; 16: 45-8.
Feigin IH, Gross SW. Sarcoma arising in glioblastoma of the brain. Am J Pathol 1958, 33: 633-53.
Rubinstein LJ. The development of contiguos sarcomatous and gliomatous tissue in intracranial tumours. J Pathol Bact 1956; 71: 441-59.
Lalitha VS, Rubinstein LJ. Reactive glioma in intracranial sarcoma: a form mixed sarcoma and glioma (sarcoglioma). Report of 8 cases. Cancer 1979; 46: 243-57.
Reis RM, Könu-Lebleblicioglu D, Lopes JM, Kleihues P, Ohgaki H. Genetic Profile of Gliosarcomas. Am J Pathol 2000; 156: 425-32.
Smith TW, Tyler HR, SChoene WC. Atypical astrocytes and Rosenthal fibers in a case of amyotrophic lateral sclerosis associated with a cerebral glioblastoma multiforme. Acta Neuropathol 1975; 31: 29-34.
Del Bigio MR, Deck. Rosenthal fibers producing a granular cell appearance in a glioblastoma. Acta Neuropathol 1993; 86: 100-4.
Ozolek JA, Finkelstein SD, Couce ME. Gliosarcoma with epithelial differentiation: immunohistochemical and molecular characterization. A case report and review of the literature. Mod Pathol 2004; 17, 739-45.
Kim DS, Kang SK, Chi JG. Gliosarcoma: A Case with Unusual Epithelial Feature. J Korean Med Sci 1999; 14: 345-50.
Galanis E, Buckner JC, Dinapoli RP, Scheithauer BW, Jenkin RB, Wang CH, et al. Clinical outcome of gliosarcoma compared with glioblastoma multiforme. North Central Cancer Treatment Group results. J Neurosurg 1998; 89: 425-30.