
Vol. 39, n.º 4, 2006
REVISTA
ESPAÑOLA DE
Vol. 39, n.º 4, 2006 |
REVISIONES
Artemio Payá Romá1, Cristina Alenda González1, Rodrigo Jover Martínez2, F. Ignacio Aranda López1
Hospital General Universitario de Alicante
1 Servicio de Patología.
2 Servicio de
Gastroenterología.
paya_art@gva.es
RESUMEN
Un 7,5% de los carcinomas colorrectales (CCR) en España presenta alteraciones del sistema de reparación de errores de replicación del ADN (mismatch repair, MMR). De ellos, un 20% se desarrolla en pacientes que presentan el síndrome de Lynch. Para identificar a estos pacientes se utilizan criterios clínicos, moleculares, histopatológicos e inmunohistoquímicos. El análisis inmunohistoquímico de las proteínas reparadoras (MLH1, MSH2, MSH6 y PMS2) ha demostrado ser una técnica válida para la detección de tumores con alteración del MMR. La generalización del uso de la inmunohistoquímica hace que actualmente el patólogo desempeñe un papel fundamental en la identificación de pacientes con síndrome de Lynch.
Palabras clave: Carcinoma colorrectal, inestabilidad de microsatélites, inmunohistoquímica, síndrome de Lynch.
SUMMARY
Colorectal carcinoma (CRC) in Spain shows mismatch-repair deficiency (MMR+) reaching a 7.5%. Twenty percent of them presents in Lynch syndrome. Identification of these patients is based on clinical, molecular, histopathologic and immunohistochemical criteria. Immunohistochemical analysis of mismatch-repair proteins (MLH1, MSH2, MSH6, and PMS2) is a valid technique to detect MMR+ tumors. The generalized use of immunohistochemistry confers to pathologists a fundamental role in the identification of patients with Lynch syndrome.
Key words: Colorrectal carcinoma, microsatellite instability, immunohistochemistry, Lynch syndrome.
INTRODUCCIÓN
El carcinoma colorrectal (CCR) es la segunda causa de muerte por cáncer en hombres y mujeres en nuestro medio después del cáncer de pulmón y de mama, respectivamente. Desde el punto de vista de las alteraciones genéticas, la mayoría (90%) de los CCR presenta activación de determinados oncogenes (K-ras) e inhibición de genes supresores (DCC, APC, TP53). Los tumores originados por esta asociación de alteraciones, denominada vía supresora, muestran entre sus características el ser aneuploides (inestabilidad cromosómica).
Existe una segunda vía oncogénica caracterizada por la alteración del sistema de reparación de errores durante la replicación del ADN, controlado por los genes MMR (mismatch repair), principalmente MLH1, MSH2, MSH6 y PMS2 . Los tumores desarrollados por esta vía presentan cientos de mutaciones en secuencias altamente repetitivas denominadas microsatélites. Para denominarlos se han aplicado en la literatura diversos términos como tumores con inestabilidad de microsatélites (IMS+), tumores con alteración de la vía reparadora (MMR+), tumores con fenotipo RER+ (replication errors) o tumores con fenotipo mutador.
Los tumores MMR+ presentan un mejor pronóstico que los tumores sin alteración de la vía reparadora . Además, no se benefician de los tratamientos quimioterápicos basados en terapias con 5-fluorouracilo.
La IMS se observa en el 7,4% de los CCR de población no seleccionada en España. La gran mayoría de tumores con IMS (83% aproximadamente) son esporádicos, y el 17% restante se desarrolla en pacientes con Carcinoma Colorrectal Hereditario no Polipósico (CCHNP) o síndrome de Lynch.
CARACTERÍSTICAS HISTOPATOLÓGICAS
Los tumores MMR+ muestran una localización predominante en colon derecho (proximales a ángulo esplénico) y presentan algunos rasgos histológicos característicos, que ayudan a su identificación.
Tipo histológico
Un 44% de tumores MMR+ presenta tipos histológicos especiales. El más frecuente es el carcinoma mucinoso que supone un 34% de los tumores inestables. Además, en este tipo histológico la frecuencia está relacionada con su localización: son inestables un 60% de los tumores mucinosos localizados en el lado derecho y tan solo un 20% de los localizados en el izquierdo. El segundo tipo en frecuencia es el carcinoma medular (8%). Prácticamente todos los carcinomas medulares son MMR+. El carcinoma de células en anillo de sello es un tipo histológico raro que se asocia a inestabilidad en un 25% de casos y supone un 2,2% del total de tumores IMS+. Un aspecto frecuente en los tumores IMS+ es la combinación de varios tipos histológicos con transiciones abruptas entre ellos, patrón observado en un 45% de casos (fig. 1).
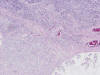
Fig. 1:
CCR con patrón histopatológico mixto. Carcinoma
de células en anillo de sello, carcinoma medular y carcinoma mucinoso.
Linfocitosis intratumoral
La mayoría de los tumores MMR+ presenta linfocitosis intratumoral (79%). Aunque el porcentaje varía según el autor, la presencia de 3 o más linfocitos intraepiteliales por campo de gran aumento está altamente asociada al fenotipo MMR+. Si además el tumor presenta cualquier grado de diferenciación mucinosa o ausencia de necrosis intraglandular, la sensibilidad para la detección del fenotipo MMR+ es del 100%. En las áreas adenomatosas o de carcinoma in situ la linfocitosis intraepitelial no se asocia a inestabilidad y por tanto deben evitarse estas zonas para su valoración.
Margen expansivo
El 60% de los tumores MMR+ tiene margen expansivo. El margen de crecimiento tiene un valor pronóstico importante, por lo que la frecuente presencia de un crecimiento expansivo puede explicar en parte el mejor pronóstico asociado a los tumores inestables.
También se ha asociado al fenotipo MMR la reacción linfoide peritumoral tipo Crohn con folículos linfoides prominentes y la ausencia de necrosis intraglandular.
Una vez que se saben identificar las características asociadas a la inestabilidad, la impresión subjetiva del patólogo tiene un valor mayor que cualquiera de las características analizadas de forma individual para la detección de tumores MMR+.
SÍNDROME DE LYNCH
El síndrome de Lynch es el síndrome de CCR hereditario más frecuente. Muestra un patrón de herencia autosómica dominante y representa del 0,9-2% de todos los CCR . Se caracteriza por mutaciones germinales en alguno de los genes MMR (MLH1 50%, MSH2 39%, MSH6 7%, PMS2<4%). Los pacientes afectos muestran una predisposición a desarrollar diversos tumores, normalmente a temprana edad. Los más frecuentes son el carcinoma de colon, endometrio y estómago. Otros tumores asociados son de intestino delgado, vía biliar, ovario, uréter, pelvis renal, cerebro y adenomas sebáceos cutáneos.
Los tumores desarrollados presentan IMS y pérdida de expresión inmunohistoquímica (IHQ) de la proteína mutada en la mayor parte de casos.
Originalmente el diagnóstico de HNPCC era clínico y se basaba en los criterios de Ámsterdam, publicados en 1990 . En 1999 se ampliaron estos criterios (Ámsterdam II) añadiendo el resto de tumores asociados al síndrome (tabla 1). Aun con los criterios ampliados, la mayoría de pacientes con síndrome de Lynch (mutación germinal identificada) no cumple los criterios de Ámsterdam.

Para identificar un mayor número de pacientes afectos se crearon los criterios de Bethesda revisados (tabla 1). Estos criterios son menos restrictivos que los de Ámsterdam y se utilizan para seleccionar aquellos pacientes en los que debe realizarse el estudio de las alteraciones del MMR (análisis de microsatélites y/o inmunohistoquímica). Es importante destacar que uno de los criterios de Bethesda se basa en rasgos histopatológicos frecuentemente asociados a IMS (fig. 2).
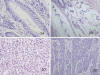
Fig. 2:
Características morfológicas incluidas en los
criterios de Bethesda Revisados. CCR con linfocitosis intraepitelial (2A),
diferenciación mucinosa (2B), células en anillo de sello (2C) o patrón de
crecimiento medular (2D).
Aunque inicialmente considerados como muy específicos, recientes estudios han demostrado que sólo el 60% de los pacientes que cumple los criterios de Ámsterdam tiene mutaciones germinales en los genes MMR. Al grupo de pacientes que cumple estos criterios sin mutaciones germinales se le ha denominado por algunos autores CCR Familiar tipo X. No se conoce actualmente el sustrato genético de este síndrome.
FORMAS DE DETECCIÓN DE TUMORES MMR+
El estudio de las alteraciones del mecanismo de reparación puede realizarse a tres niveles: a) estudiando los genes directamente b) analizando la expresión de las proteínas codificadas o c) analizando microsatélites, que son la diana final donde actúan las proteínas reparadoras. Como el análisis de mutaciones germinales es costoso, habitualmente se seleccionan los pacientes con tumores MMR+ mediante el análisis de microsatélites y el análisis inmunohistoquímico.
Análisis de mutaciones germinales
El estudio se realiza mediante análisis de secuenciación y estudio de grandes reordenamientos en ADN genómico. En muchos centros se comienza con la detección de reordenamientos genómicos, por tratarse de una técnica relativamente sencilla y en caso de detectarse se obvia el cribado posterior de mutaciones. La detección de la mutación permite identificar a los portadores asintomáticos e incluirlos en los programas de detección precoz.
Análisis de microsatélites
En 1998 se acordó un panel de 5 marcadores microsatélites consenso (tabla 2) y los criterios para definir la inestabilidad. Se considera que un tumor presenta alta IMS (IMS-H) si muestra inestabilidad en 2 o más marcadores y baja IMS (IMS-L) si aparece en un marcador. Actualmente tiende a abandonarse el concepto de IMS-L porque se ha demostrado que este grupo presenta características superponibles a las de los tumores sin IMS. Excepto que se especifique lo contrario, el término IMS+ se refiere a los antes denominados IMS-H.

El análisis se realiza mediante PCR comparando en cada caso el tamaño de los alelos del tumor con su correspondiente ADN no tumoral. En los tumores con IMS pueden observarse con los marcadores dinucleótidos inserciones o deleciones en el ADN tumoral, mientras que con los mononucleótidos siempre son deleciones. Los marcadores más sensibles a la inestabilidad son los mononucleótidos. En concreto con el BAT26 pueden detectarse más del 95% de tumores con IMS, por lo que en algunos trabajos se ha utilizado como único marcador. Tiene además la ventaja de que es prácticamente monomórfico, lo cual permite utilizar sólo ADN tumoral sin necesidad de comparar con ADN no tumoral. Todo ello simplifica la técnica, abarata costes y además permite realizar el análisis cuando no se dispone de tejido no tumoral (ej. biopsias endoscópicas). Actualmente se está planteando la necesidad de modificar los microsatélites utilizados en el panel consenso, aumentando el número de marcadores mononucleótidos por ser los más sensibles.
Análisis inmunohistoquímico
Bases moleculares de la inmunohistoquímica
El sistema MMR está controlado fundamentalmente por las proteínas MLH1, MSH2, MSH6 y PMS2. Entre ellas forman complejos heterodiméricos. El más abundante y primero en actuar está formado por MSH2-MSH6. A este complejo se le une posteriormente otro formado por MLH1-PMS2 . El complejo final escinde el error del ADN y lo repara. Si ambos alelos de alguno de estos genes se inactivan por cualquier mecanismo (deleción, mutación o metilación), los errores de replicación no se pueden reparar y se acumularán mutaciones en microsatélites, produciéndose IMS y desarrollándose el CCR. La inactivación de ambos alelos tiene como consecuencia la pérdida de expresión de la proteína, lo cual puede detectarse mediante inmunohistoquímica.
Los tumores esporádicos MMR+ se originan debido a inactivación por hipermetilación del promotor del gen MLH1. En estos casos siempre se observa pérdida de expresión inmunohistoquímica de MLH1.
En los tumores del síndrome de Lynch puede observarse pérdida de expresión de cualquiera de las proteínas MMR (MLH1 50%, MSH2 39%, MSH6 7%, PMS2<4%). Un mínimo porcentaje (5% aproximadamente) de pacientes con mutación germinal puede mostrar expresión conservada de las cuatro proteínas. Esto puede ser debido a la expresión de una proteína no funcional pero con conservación del epítopo reconocido por el anticuerpo, o bien, que la mutación esté en alguno de los otros genes que controlan el MMR (PMS1 o MLH3).
La pérdida de expresión de MLH1 generalmente se asocia a pérdida secundaria de PMS2. De la misma forma, la pérdida de MSH2 suele asociarse a pérdida secundaria de MSH6. Las pérdidas aisladas de PMS2 o MSH6, indicativas de mutación en estos genes, son poco frecuentes y sólo deben considerarse tras haber observado expresión de MLH1 y MSH2.
Forma de valoración de la inmunohistoquímica
El estudio inmunohistoquímico se realiza sobre tejido fijado en formol e incluido en parafina. Para su valoración siempre se dispone de controles internos positivos (estroma, linfocitos), necesarios para poder determinar que la ausencia de expresión en un tumor no es debida a un problema de la técnica. Un caso se considera con pérdida de expresión cuando no se observa inmunotinción en ninguna célula neoplásica. Frecuentemente la tinción obtenida es heterogénea. Por ello, siempre se debe valorar la pérdida de expresión en un campo de gran aumento que disponga de controles internos positivos (fig. 3).
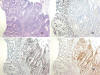
Fig. 3:
Carcinoma colorrectal con pérdida de expresión de
MLH1. 3A) H&E 200x. 3B) Pérdida de expresión de MLH1 200x (BD Pharmingen, clon
G168-15, dilución 1:30). 3C) Expresión conservada de MSH2 200x (BD Transduction
Laboratorios, clon 44, dilución 1:100). 3D) Expresión conservada de MSH6 200x
(Calbiochem, clon FE11, dilución 1:30). Este caso mostraba también pérdida de
expresión secundaria de PMS2 (BD Pharmingen, clon A16-4, dilución 1:100).
El resultado inmunohistoquímico debe expresarse como presencia o ausencia de expresión de cada una de las proteínas o como no valorable si no se obtienen controles internos adecuados. No deben establecerse valoraciones semicuantitativas basadas en la intensidad y porcentaje de inmunotinción porque se ha demostrado que esta semicuantificación no se correlaciona con la presencia de inactivación génica. Los términos positivo y negativo también deben evitarse, ya que pueden inducir a confusión.
Limitaciones de la inmunohistoquímica
En ocasiones existen limitaciones técnicas que dificultan la valoración de la inmunohistoquímica. Entre las más importantes están los problemas de fijación del tejido, el anticuerpo utilizado o la pérdida de antigenicidad en cortes almacenados más de 24 horas antes de la realización de la técnica. Las piezas de resección colorrectal si no son abiertas inmediatamente tras la cirugía, pueden presentar problemas de fijación.
Para detectar los casos de CCR esporádicos con IMS, la inmunohistoquímica tiene una sensibilidad y especificidad del 100%. En cambio, en el síndrome de Lynch, hasta en un 5% de los tumores no se detecta pérdida de expresión del gen mutado. Para detectar estos casos se hace necesario recurrir al análisis de microsatélites.
¿QUÉ MÉTODO UTILIZAR?
Tanto la IHQ como el análisis de microsatélites son técnicas igualmente válidas para el despistaje de tumores con fenotipo mutador y por tanto para la detección de pacientes con síndrome de Lynch. La IHQ como método inicial tiene la ventaja de que es una técnica sencilla y barata, fácilmente realizable en cualquier laboratorio en el que se hagan rutinariamente tinciones inmunohistoquímicas como es el caso de la mayoría de servicios de Anatomía Patológica. El análisis de microsatélites requiere un mayor equipamiento técnico, no disponible en todos los centros. Además, la inmunohistoquímica permite identificar la proteína no expresada y, por tanto, el gen afectado. También se ha visto que en tumores mucinosos la sensibilidad de la inmunohistoquímica es mucho mayor que el análisis de microsatélites debido a la baja densidad de células tumorales, que dificulta la obtención de suficiente ADN para el estudio.
INDICACIONES PARA EL ANÁLISIS DEL FENOTIPO MUTADOR
Actualmente está consensuado que se realice el análisis de alteraciones del MMR en los pacientes que cumplan criterios de Bethesda revisados o Ámsterdam II. Recientemente se ha observado que hasta un 21% de pacientes con síndrome de Lynch no cumple criterios de Ámsterdam o Bethesda. Por esto, algunos autores opinan que, dado el bajo coste de la inmunohistoquímica, debería realizarse de forma rutinaria a todos los CCR, no sólo a los pacientes que cumplen los criterios clínicos. Nuestro grupo es de esta opinión y actualmente estamos realizando el análisis inmunohistoquímico a todos los CCR sin ningún criterio de selección.
¿QUÉ PROTEÍNAS ESTUDIAR?
Las proteínas que más frecuentemente muestran pérdida de expresión son MLH1 y MSH2. En ocasiones se hace necesaria la valoración de MSH6 y PMS2, bien para confirmar la pérdida de las primeras en casos dudosos, o bien para detectar mutaciones aisladas de MSH6 o PMS2. Un 72% de pacientes con tumores IMS+ y sin pérdida de expresión de MLH1, MSH2 o MSH6 muestra pérdida de PMS2. Analizar las cuatro proteínas en un primer tiempo tiene un coste en tiempo y reactivos proporcionalmente menor que si se realizan primero MLH1/MSH2 y después MSH6/PMS2. Nuestro grupo ha realizado el estudio inmunohistoquímico en 1912 casos de CCR no seleccionados. En 125 casos (6,5%) se detectó pérdida de expresión de alguna de las proteínas: 96 MLH1 (77%), 24 MSH2 (19%), 3 MSH6 (2,4%) y 1 PMS2 (0,8%). En tan sólo un caso (0,8%) se detectó pérdida de MLH1 y MSH2.
IDENTIFICACIÓN DEL SÍNDROME DE LYNCH MEDIANTE INMUNOHISTOQUÍMICA
Teniendo en cuenta que la inmunohistoquímica es una técnica disponible en todos los servicios de Patología y que tiene una alta concordancia con la IMS, un posible algoritmo para detectar pacientes con síndrome de Lynch, sin conocer la historia oncológica, es el que se propone en la figura 4. Ante un CCR se realiza el estudio inmunohistoquímico de las cuatro proteínas. En tumores con pérdida de expresión de MLH1, dado que la mayoría son esporádicos, el criterio para realizar o no el análisis germinal se basa en el cumplimiento de los criterios clínicos. Una alternativa para los centros que dispongan de la técnica, es el análisis de la mutación BRAF. Recientemente se ha demostrado que los tumores esporádicos presentan la mutación V600E en el gen BRAF, la cual está ausente en los casos con mutación germinal. Los casos con presencia de mutación del gen BRAF, por tanto, pueden excluirse del análisis germinal. En tumores con pérdida de MSH2, así como con pérdidas aisladas de PMS2 o MSH6, se realiza directamente la búsqueda de mutaciones germinales de la proteína no expresada, ya que en los tumores esporádicos nunca se inactivan estos genes. En los casos en los que no se detecte pérdida de expresión pero el paciente cumpla criterios clínicos hay que realizar el análisis de microsatélites, para detectar el pequeño porcentaje de tumores inestables sin pérdida de expresión proteica asociada.
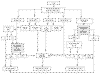
Fig. 4:
Algoritmo para identificación de síndrome de
Lynch partiendo del análisis inmunohistoquímico.
En resumen, el patólogo desempeña un papel fundamental en la identificación de pacientes con síndrome de Lynch, reconociendo las características histopatológicas asociadas a los tumores inestables e interpretando, en el contexto clínico, el análisis inmunohistoquímico de las proteínas reparadoras. El estudio inmunohistoquímico permite dirigir la búsqueda al gen afecto, disminuyendo los costes del análisis genético y aumentando el número de pacientes con síndrome de Lynch.
BIBLIOGRAFÍA
Peltomaki P, Vasen H. Mutations as-sociated with HNPCC predisposition. Update of ICG-HNPCC/INSiGHT mutation database. Dis Markers 2004; 20: 269-76.
Thibodeau SN, French AJ, Cunning-ham JM, Tester D, Burgart LJ, Roche PC, et al. Microsatellite instability in colorectal cancer: different mutator phenotypes and the principal involvement of hMLH1. Cancer Res 1998; 58: 1713-8.
Popat S, Hubner R, Houlston RS. Systematic review of microsatellite instability and colorectal cancer prognosis. J Clin Oncol 2005; 23: 609-18.
Ribic CM, Sargent DJ, Moore MJ, Thi-bodeau SN, French AJ, Goldberg RM, et al. Tumor microsatellite-instability status as a predictor of benefit from fluorouracil-based adjuvant chemotherapy for colon cancer. N Engl J Med 2003; 349: 247-57.
Carethers JM, Smith EJ, Behling CA, Nguyen L, Tajima A, Doctolero RT, et al. Use of 5-fluorouracil and survival in patients with microsatellite-unstable colorectal cancer. Gastroenterology 2004; 126: 394-401.
Jover R, Zapater P, Castells A, Llor X, Andreu M, Cubiella J, et al. Mismatch repair status in the prediction of benefit from adjuvant fluorouracil chemotherapy in colorectal cancer. Gut 2006; 55: 848-55.
Pinol V, Castells A, Andreu M, Castellvi-Bel S, Alenda C, Llor X, et al. Accu-racy of revised Bethesda guidelines, microsat-ellite instability, and immunohistochemistry for the identification of patients with hereditary nonpolyposis colorectal cancer. Jama 2005; 293: 1986-94.
Hampel H, Frankel WL, Martin E, Arnold M, Khanduja K, Kuebler P, et al. Screening for the Lynch syndrome (hereditary nonpolyposis colorectal cancer). N Engl J Med 2005; 352: 1851-60.
Jass JR, Do KA, Simms LA, Iino H, Wynter C, Pillay SP, et al. Morphology of spo-radic colorectal cancer with DNA replication errors. Gut 1998; 42: 673-9.
Smyrk TC, Watson P, Kaul K, Lynch HT. Tumor-infiltrating lymphocytes are a marker for microsatellite instability in colorectal carcinoma. Cancer 2001; 91: 2417-22.
Paya A, Alenda C, Jover R, Peiro F, Grupo de Oncologia Digestiva, AEG. Clinico-pathologic Differences Regarding MLH1 and MSH2 Expression in Microsatellite Instability (MSI) Colorectal Carcinoma. Mod Pathol 2004; 17(S 1): 127A.
Wright CL, Stewart ID. Histopathology and mismatch repair status of 458 consecutive colorectal carcinomas. Am J Surg Pathol 2003; 27: 1393-406.
Ogino S, Brahmandam M, Cantor M, Namgyal C, Kawasaki T, Kirkner G, et al. Dis-tinct molecular features of colorectal carcinoma with signet ring cell component and colorectal carcinoma with mucinous component. Mod Pathol 2006; 19: 59-68.
Young J, Simms LA, Biden KG, Wynter C, Whitehall V, Karamatic R, et al. Features of colorectal cancers with high-level microsatellite instability occurring in familial and sporadic settings: parallel pathways of tumorigenesis. Am J Pathol 2001; 159: 2107-16.
Greenson JK, Bonner JD, Ben-Yzhak O, Cohen HI, Miselevich I, Resnick MB, et al. Phenotype of microsatellite unstable colorectal carcinomas: Well-differentiated and focally mucinous tumors and the absence of dirty necrosis correlate with microsatellite instability. Am J Surg Pathol 2003; 27: 563-70.
Jass JR. HNPCC and sporadic MSI-H colorectal cancer: a review of the morphological similarities and differences. Fam Cancer 2004; 3: 93-100.
Alexander J, Watanabe T, Wu TT, Rashid A, Li S, Hamilton SR. Histopathological identification of colon cancer with microsatellite instability. Am J Pathol 2001; 158: 527-35.
Aaltonen LA, Sankila R, Mecklin JP, Jarvinen H, Pukkala E, Peltomaki P, et al. A novel approach to estimate the proportion of hereditary nonpolyposis colorectal cancer of total colorectal cancer burden. Cancer Detect Prev 1994; 18: 57-63.
Lynch HT, de la Chapelle A. Hereditary colorectal cancer. N Engl J Med 2003; 348: 919-32.
Vasen HF, Mecklin JP, Khan PM, Lynch HT. The International Collaborative Group on Hereditary Non-Polyposis Colorectal Cancer (ICG-HNPCC). Dis Colon Rectum 1991; 34: 424-5.
Vasen HF, Watson P, Mecklin JP, Lynch HT. New clinical criteria for hereditary nonpolyposis colorectal cancer (HNPCC, Lynch syndrome) proposed by the International Collaborative group on HNPCC. Gastroenterology 1999; 116: 1453-6.
Umar A, Boland CR, Terdiman JP, Syngal S, de la Chapelle A, Ruschoff J, et al. Revised Bethesda Guidelines for hereditary nonpolyposis colorectal cancer (Lynch syn-drome) and microsatellite instability. J Natl Cancer Inst 2004; 96: 261-8.
Lindor NM, Rabe K, Petersen GM, Haile R, Casey G, Baron J, et al. Lower cancer incidence in Amsterdam-I criteria families without mismatch repair deficiency: familial colorectal cancer type X. Jama 2005; 293: 1979-85.
Boland CR, Thibodeau SN, Hamilton SR, Sidransky D, Eshleman JR, Burt RW, et al. A National Cancer Institute Workshop on Microsatellite Instability for cancer detection and familial predisposition: development of international criteria for the determination of microsatellite instability in colorectal cancer. Cancer Res 1998; 58: 5248-57.
Loukola A, Eklin K, Laiho P, Salovaara R, Kristo P, Jarvinen H, et al. Microsatellite marker analysis in screening for hereditary nonpolyposis colorectal cancer (HNPCC). Cancer Res 2001; 61: 4545-9.
Kunkel TA, Erie DA. DNA mismatch repair. Annu Rev Biochem 2005;74: 681-710.
Ruszkiewicz A, Bennett G, Moore J, Manavis J, Rudzki B, Shen L, et al. Correlation of mismatch repair genes immunohistochemistry and microsatellite instability status in HNPCC-associated tumours. Pathology 2002; 34: 541-7.
Halvarsson B, Lindblom A, Rambech E, Lagerstedt K, Nilbert M. Microsatellite insta-bility analysis and/or immunostaining for the diagnosis of hereditary nonpolyposis colorectal cancer? Virchows Arch 2004; 444: 135-41.
Plaschke J, Kruger S, Pistorius S, Theissig F, Saeger HD, Schackert HK. In-volvement of hMSH6 in the development of hereditary and sporadic colorectal cancer re-vealed by immunostaining is based on germ-line mutations, but rarely on somatic inactiva-tion. Int J Cancer 2002; 97: 643-8.
Plaschke J, Kruger S, Jeske B, Theis-sig F, Kreuz FR, Pistorius S, et al. Loss of MSH3 protein expression is frequent in MLH1-deficient colorectal cancer and is associated with disease progression. Cancer Res 2004; 64: 864-70.
Niessen RC, Berends MJ, Wu Y, Si-jmons RH, Hollema H, Ligtenberg MJ, et al. Identification of mismatch repair gene muta-tions in young colorectal cancer patients and patients with multiple HNPCC-associated tu-mours. Gut 2006; 55: 1781-8.
Jover R, Paya A, Alenda C, Poveda MJ, Peiro G, Aranda FI, et al. Defective mis-match-repair colorectal cancer: clinicopa-thologic characteristics and usefulness of im-munohistochemical analysis for diagnosis. Am J Clin Pathol 2004; 122: 389-94.
Gill S, Lindor NM, Burgart LJ, Smalley R, Leontovich O, French AJ, et al. Isolated loss of PMS2 expression in colorectal cancers: frequency, patient age, and familial aggregation. Clin Cancer Res 2005; 11: 6466-71.
Domingo E, Niessen RC, Oliveira C, Alhopuro P, Moutinho C, Espin E, et al. BRAF-V600E is not involved in the colorectal tumorigenesis of HNPCC in patients with functional MLH1 and MSH2 genes. Oncogene 2005; 24: 3995-8.
Domingo E, Espin E, Armengol M, Oliveira C, Pinto M, Duval A, et al. Activated BRAF targets proximal colon tumors with mis-match repair deficiency and MLH1 inactivation. Genes Chromosomes Cancer 2004; 39: 138-42.
Domingo E, Laiho P, Ollikainen M, Pinto M, Wang L, French AJ, et al. BRAF screening as a low-cost effective strategy for simplifying HNPCC genetic testing. J Med Genet 2004; 41: 664-8.