
Vol. 39, n.º 4, 2006
REVISTA
ESPAÑOLA DE
Vol. 39, n.º 4, 2006 |
REVISIONES
Beatriz Eizaguirre Zarza1, Juan José Burgos Bretones2
1 Hospital de
Galdakao.
2 Hospital de Cruces.
beizaguirre@hgda.osakidetza.net
RESUMEN
El tumor estromal gastrointestinal (GIST) es el tumor mesenquimal más frecuente en el tracto digestivo. La mayoría de los GIST poseen una característica mutación con ganancia de función del gen c-KIT, que codifica el receptor KIT para el factor de células Stem. El reconocimiento de este tumor ha adquirido más importancia tras la disponibilidad de un inhibidor de la tirosina quinasa KIT, mesilato de Imatinib, llamado comercialmente Glivec (Novartis-Pharma, Basilea, Suiza), en el tratamiento de los tumores metastásicos e irresecables.
El propósito de este trabajo es la revisión de la patología, pronóstico y tratamiento de los tumores GIST.
Palabras clave: GIST, aparato digestivo, kit, CD117, tratamiento, pronóstico.
SUMMARY
GIST is the most common mesenchymal tumor in the digestive tract. The mayority of them has characteristic gain-of-function mutations of the c-kit gene, which encodes the KIT Receptor for stem cell factor. The specific identification of GIST has become more important after the availability of KIT-selective tyrosine kinase inhibitor Imatinib mesylate, STI571, commercially known as Gleevec (Novartis-Pharma, Basel, Switzerland) in the treatment of unresectable and metastatic tumors.
The purpose of this article is to review data of the pathology, prognosis and management of GIST.
Key words: GIST, digestive tract, c-KIT, CD117, treatment, prognosis.
INTRODUCCIÓN
En la actualidad, se denomina GIST a los tumores mesenquimales CD117 positivos, fusiformes o epitelioides, primarios de tracto digestivo, mesenterio, y retroperitoneo.
Este término se utilizó por vez primera en 1983. Mazur y Clark lo emplearon para designar unos tumores no epiteliales del tubo digestivo, que carecían de rasgos ultraestructurales de músculo liso y características inmunohistoquímicas de célula de Schwann (1).
Es el sarcoma más frecuente del tracto gastrointestinal (TGI). Supone el 2% de tumores a este nivel, pero el 80% de los sarcomas gastrointestinales.
Su incidencia es de 10 a 20 casos por millón de habitantes. Teniendo una prevalencia mayor, debido el curso clínico largo de la enfermedad (10-15 años) (2,3).
La incidencia máxima es entre la 4.ª y 6.ª décadas, siendo la distribución por géneros semejante. Aunque estudios recientes sugieren una incidencia algo superior en varones (3).
GIST comparte similitudes inmunofenotípicas con las células intersticiales de Cajal, localizadas alrededor del plexo mientérico, y dispersas en la muscular propia (4).
Características como la expresión de KIT, CD34, la cadena pesada de la miosina de músculo liso y la nestina (5), son comunes en ambos.
Las células intersticiales de Cajal actúan como marcapasos intermediarios entre sistema nervioso y sistema de músculo liso. Expresan CD117, en el 95% de los casos igual que los GIST, y poseen una mezcla de rasgos neurales y miógenos en la ultraestructura.
Kinblom, en 1998, sugirió que los GIST se originaban de una célula madre que se diferenciaba hacia célula intersticial de Cajal. La hipótesis de la célula precursora explicaría por qué tumores mesenquimales con histología similar a los GIST, CD117 positivos, pueden aparecer en epiplon y mesenterio.
No existe una evidencia final que permita considerar estas células como precursoras de los GIST. La posibilidad de que posean un precursor más inmaduro es un debate abierto aún, hoy en día.
La expresión de KIT es necesaria para el desarrollo embriológico de melanocitos, gametocitos, mastocitos, y células intersticiales de Cajal (6).
PERSPECTIVA GENERAL
Kinblom y colaboradores llevaron a cabo un estudio poblacional, reuniendo datos epidemiológicos y de pronóstico de los GIST (7). En una población de Suecia de 1,3-1,6 millones de habitantes, con 4 hospitales de referencia, investigaron tumores mesenquimales, c-KIT positivos entre 1983 y 2000.
Estudiaron 650 casos de los cuales 398 cumplían los criterios diagnósticos de GIST. El 72% de los casos de GIST, habían sido diagnosticados de otra forma. El 28% se diagnosticó como GIST, un 34% leiomiomas, un 18% leiomiosarcomas, 13% leiomioblastomas, y un 7% otros diagnósticos.
En cuanto a la presentación clínica, el 69% fueron sintomáticos, siendo la mayoría de estos síntomas inespecíficos: dolor vago, anorexia, anemia, pérdida de peso, náuseas… Menos frecuentes fueron la hemorragia gastrointestinal (por ulceración mucosa), o intraperitoneal (por rotura tumoral).
Se pueden localizar en el TGI, o en mesenterio, o retroperitoneo. Entre el 50-60% casos se dan en el estómago, el 20-30% en intestino delgado, el colon supone el 10% aproximadamente, y el 15% restante otros: recto, esófago, mesenterio, retroperitoneo. Siendo el esófago el 5% de los casos. Tal y como describe Kindblom en su estudio (2,3).
El aspecto macroscópico depende del tamaño, que oscila entre 1 y 32 cm, aunque la mayoría tienen más de 2 cm. Aparecen como nódulos serosos, intramurales o submucosos. Los grandes suelen mostrar un crecimiento exofítico, hacia la luz, con ulceración (20-30% casos) o no de la mucosa. También pueden protuir hacia la serosa con gran componente extraparietal, lo que enmascara su origen digestivo en las técnicas de imagen (2,8,9) (fig. 1).
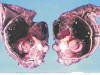
Fig. 1:
Tumoración gástrica, de crecimiento endofítico. Muestra una consistencia
sólido-quística. Se observan áreas de hemorragia y necrosis.
Al corte, son tumores bien delimitados, no encapsulados, lobulados, blanquecinos. En algunas ocasiones, sobre todo los más agresivos, suelen mostrar áreas de hemorragia, necrosis, o quistificación.
Desde el punto de vista microscópico, presentan tres patrones de crecimiento (10): expansivo, pseudoexpansivo e infiltrante. El expansivo en la muscular de la mucosa, muscular propia o serosa. El pseudoexpansivo favorece la aparición de nódulos satélite a distancia de la tumoración, lo cual dificulta la cirugía. El infiltrante, con crecimiento insidioso entre las células del meso o las fibras musculares. Este tipo de crecimiento se ha asociado a mayor agresividad, preferentemente en tumores rectales y colónicos (11).
Histológicamente se distinguen tres patrones arquitecturales: fusiforme (70%) (fig. 2), epitelioide (20%) (fig. 3), y mixto (10%) (9).
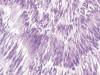
Fig. 2:
Tumor estromal gastrointestinal. Patrón
fusiforme, con empalizadas nucleares. HE 40X.
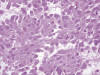
Fig. 3:
Tumor estromal gastrointestinal. Patrón epitelioide. HE 40x.
Algunos tumores presentan una densidad celular alta, lo cual se ha relacionado con mayor agresividad, por ejemplo en los estudios del grupo GEIS.
En otros, se observa una franca atipia citológica. Sobre todo epitelioides y gástricos. Curiosamente, a veces, se asocia a una escasa actividad mitótica, lo cual les hace ser menos agresivos.
En algunos tumores de ID, se observan las fibras en madeja (skenoides), estructuras fibrilares PAS positivas y eosinófilas. Fueron relacionadas con diferenciación neural, aunque parece que no tienen significado histogenético (9).
Las vacuolas paranucleares citoplasmáticas se observan en el 5% de los casos, preferentemente en GIST gástricos.
En cuanto al inmunofenotipo, la mayoría (95%) expresan CD117. Tinción difusa citoplasmática, con refuerzo de membrana o en acúmulos perigolgianos.
Otros marcadores a menudo positivos son CD34 (60-70%), Actina músculo liso (15-60%), S100 (10%), y Desmina (rara vez). Esporádicamente se ha observado expresión de NSE, neurofilamentos, cromogranina, y queratinas 8 y 18 (3,9).
Recientemente se ha descrito la expresión de DOG1 hasta en un 98% de los casos, incluso aquellos CD117 negativos. Se expresa en tumores con mutación del gen KIT y los que tienen mutación de PDGFRA. Positivo en algunos carcinomas, pero negativo en sarcomas que plantean diagnóstico diferencial con GIST. Puede resultar útil, por tanto, para diagnóstico en casos dudosos (12,13).
Se ha descrito, también, una fuerte expresión de la proteína kinasa Cq. Un marcador altamente específico y útil en el diagnóstico, especialmente de GIST c-KIT negativos (14,15).
La nestina, es un filamento intermedio tipo VI típico de células stem incluidas las de sistema nervioso y sistema muscular. Positiva en casi todos los GIST, pero también en schwannomas, melanomas, rabdomiosarcomas. Por tanto, poco específica (3).
El diagnóstico diferencial se deberá hacer con lesiones similares morfológicamente, o CD34 positivas como: tumores fibrohistiocitarios, tumores de vaina nerviosa periférica, tumor fibroso solitario, angiosarcoma, sarcoma de Kaposi, pólipo fibroide inflamatorio, tumor miofibroblástico inflamatorio… así como con tumores que expresen c-KIT: melanoma, liposarcoma desdiferenciado, carcinoma indiferenciado de células pequeñas de pulmón, condrosarcoma mixoide extraesquelético, sarcoma ewing, neuroblastoma, sarcoma granulocítico, etc. (3).
CRITERIOS DE MALIGNIDAD
Son criterios de malignidad indudables, la presencia de metástasis y/o invasión de órganos vecinos.
Tienen una importancia dudosa, la densidad celular, (factor que en los estudios del grupo GEIS tuvo una significación independiente de peor pronóstico), atipia, ulceración mucosa, infiltración muscular (factor predictivo de mal pronóstico en tumores anorectales) (16).
La invasión de la mucosa, aunque poco frecuente, se observa solo en tumores malignos, y no debe ser confundida con la ulceración mucosa, que no tiene valor predictivo (17).
El pronóstico muestra cierta asociación con la localización anatómica, con tendencia a ser de mayor malignidad los localizados en intestino delgado frente a los localizados en el estómago.
Miettinem, en un estudio de 1700 GIST gástricos, observó que el 83% eran benignos (18).
En duodeno, sin embargo, la mitad suelen ser malignos (8).
En el esófago, son poco frecuentes. Predominan los leiomiomas (8).
Pero más de la mitad de los GIST son malignos.
En cuanto a la biología molecular, Singer y colaboradores (19), evaluaron por vez primera, la importancia pronóstica de las mutaciones c-KIT en un total de 48 GIST. Encontraron que los pacientes con mutación missense de KIT en el exón 11 presentaban un porcentaje libre de recidivas a los 5 años del 89%±10%, si se comparaban con el 40%±8% de los pacientes que tenían otro tipo de mutaciones.
La positividad para CD34, p53, bcl-2, ciclina D1, c-myc, no parecen tener influencia pronóstica, aunque hay resultados contradictorios en la literatura (10,20). En algunos estudios la p53 parece tener valor predictivo pronóstico. Lo mismo que c-myc (21).
La expresión de VEGF, la pérdida de expresión de CD44 (22), y las alteraciones de la p16 se asocian a tumores de peor pronóstico (23).
Además, existen en estos tumores, una serie de marcadores genéticos, asociados a agresividad:
Delecciones 9q, 9p, pérdidas alélicas 22q son más frecuentes en tumores malignos (3,11).
Pérdidas o ganancias de material genético. Los GIST benignos tiene un número menor de copias de ADN que los malignos (24).
La actividad de la Telomerasa, mostrada sólo por GIST agresivos.
La sobreexpresión de ciertos genes, más frecuentes en GIST agresivos: VIL2, COL8A1, CCNB2, HMG2, TSG101 (10).
Lasota y colaboradores han encontrado que cierto tipo de mutaciones del dominio yuxtamembrana, más frecuentes en el estómago tiene mejor pronóstico (25).
Además, se ha descrito que mutaciones en el exón 14 del PDGFRA se relacionan con tumores GIST gástricos, preferentemente, de curso clínico más favorable y morfología epiteliode (26).
Recientemente, un estudio de Martin y colaboradores, demuestra la relevancia del tipo y la posición de las delecciones del gen KIT. Así, las anormalidades que afectan a codones 557, y 558 en el exón 11 confieren un riesgo de recidiva mayor en pacientes con GIST (27).
Además, también tuvieron significación independiente pronóstica la celularidad elevada, un índice mitótico superior a 10 mit/50 cga, y la localización intestinal.
Pero, en lo que todos los autores están de acuerdo, es en la influencia del tamaño tumoral, y el índice mitótico en la agresividad de estos tumores. De tal forma que en 2001 se llegó a un consenso estableciéndose cuatro grupos pronósticos en función de estos dos factores (9).
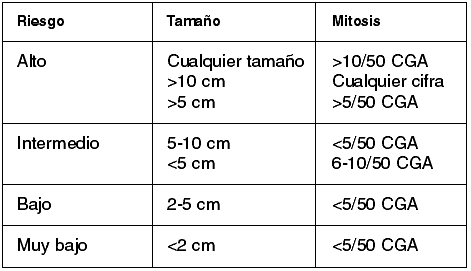
Y estos cuatro grupos de riesgo se correlacionaban con el pronóstico tal y como señaló Kinblom (7).
Otra técnica utilizada ha sido la determinación de la proliferación celular medida con la tinción de ki67. De tal forma que tumores con índice del 10% o más se asocian a mal pronóstico.
En este sentido, Kinblom, estableció un «score» que venía determinado por la suma del tamaño en cm, más el índice ki67. Ambos factores con valor predictivo independiente en su trabajo.
De tal forma, que tumores con un índice mayor de 7, tenían una supervivencia de 28 meses. Mientras que, aquellos tumores cuyo «score» era menor o igual a 7, tenían una supervivencia de 87 meses.
BIOLOGÍA MOLECULAR
Un aspecto fundamental de los tumores GIST son las mutaciones con ganancia de función del gen KIT, que pueden tener lugar en diferentes exones (4,28,29).
Lasota y colaboradores encontraron que las mutaciones de c-KIT eran más frecuentes en tumores malignos que benignos, y que no aparecían nunca en leiomiomas, o leiomiosarcomas (30).
Sin embargo, la mayoría de estos primeros trabajos estaban basados en series retrospectivas, y en ellas la incidencia de mutaciones podría estar infrarepresentada.
Así, Corless detectó un 83% de mutaciones en un estudio molecular de 13 GIST de menos de 1cm, hallazgo incidental. Dada esta alta incidencia el valor de estos hallazgos tendría escasa relevancia. Por tanto, son un evento oncogénico precoz, y por sí mismas no tienen influencia pronóstica (31).
Sin embargo, sí la tiene el tipo y/o la localización de la mutación (19,32).
Parece ser que los distintos tipos de mutaciones del gen KIT confieren diferentes grados de activación, lo cual se traduciría en diferencias en cuanto a la agresividad del tumor.
Las mutaciones se dan, en el 67,5% de los casos, a nivel del exón 11, en el dominio yuxtamembrana, y en el 11% de los casos a nivel del exon 9, en el dominio extracelular.
En el exon 13, se dan en un 0,9% de los casos, y en el 17, en el 0,5% de los casos (5,33).
1. Mutaciones exón 11
Se pueden encontrar tres tipos de mutaciones (5). Las más comunes son las delecciones intersticiales que suelen afectar a la parte inicial del exón (ente los codones 550-560). Con menor frecuencia se encuentran mutaciones puntuales que por lo general se limitan a cuatro codones: 557, 559, 560 y 576. Y en menor proporción de casos, al final del exón se suelen encontrar duplicaciones en tandem, en un determinado número de codones (25).
2. Mutaciones en el exón 9
De forma mayoritaria se encuentra un tipo de mutación correspondiente a la inserción de 6 nucleótidos, que resulta en la duplicación de los aminoácidos Alanina 501 y Tirosina 502. Este tipo de mutaciones son más frecuentes en GIST de localización intestinal.
3. Mutaciones en el exón 13
Hasta el momento sólo se han encontrado mutaciones missense resultando en la sustitución de ácido glutámico por lisina en la posición 642 (K642E).
4. Mutaciones en el exón 17
Se han descrito hasta el momento mutaciones puntuales que corresponden a las sustituciones N822H y N822K. Se ha descrito otra mutación en el exón 17 asociado a GIST familiares: D820Y.
Una curiosidad es que las mutaciones missense Asp816 son frecuentes en otras neoplasias como las mastocitosis, el seminoma y el disgerminoma, la leucemia mieloide aguda y el linfoma T.
Algunos GIST carecen de mutaciones del gen KIT. Y hasta en un 35 % de ellos se observan mutaciones en el PDGFRA, que suponen el 5-7% de los casos (26,34).
El exon 18 es el más comúnmente afectado 6,3% de los casos, le sigue en frecuencia el exon 12 (0,9%), y el exón 14 (0,3%).
Existen unos 289 GIST publicados en la literatura con mutaciones PDGFRA. De los cuales el 62,6% contiene una sustitución que afecta al codón D842, en el exón 18, que son resistentes a tratamiento con Glivec® (35).
Se ha dicho que ambos son mecanismos mutuamente excluyentes (24). Sin embargo recientemente se ha descrito algún caso con ambas mutaciones (36).
Las mutaciones KIT ocurren tempranamente en el desarrollo de los GIST pero no son suficientes por sí solas para inducir malignidad.
Se han descrito cambios citogenéticos secundarios que se correlacionan con el pronóstico. Así, delecciones 14q y 22q se dan tanto en tumores benignos como malignos, sugiriendo que la pérdida de ciertos genes supresores podría tener papel en los cambios genéticos (3,5,10).
Se han descrito, por tanto, delecciones 14q y 22q, además de otra serie de cambios asociados a mayor agresividad, como son: ganancias de DNA, amplificaciones 5p, 8q, 17q, 20q, y pérdidas de 9p y 13q (28).
El-Rifai, en un estudio de 95 GIST, observó la existencia de hasta 2,6 aberraciones cromosómicas en GIST benignos, 7,5 en tumores primarios agresivos, y hasta 9 aberraciones en tumores metastásicos (37).
DIAGNÓSTICO
La ecografía suele ser la técnica inicial de diagnóstico en muchos pacientes con tumores GIST. Suelen ser tumores grandes de baja ecogenicidad (1,35,38,39).
Algunos, aparecen en estudios de endoscopia como tumores submucosos, con o sin ulceración de la mucosa. En caso de observar una de éstas, es necesario realizar una ecoendoscopia para observar la afectación zonal del tumor
Estudios recientes sugieren que la ecografía podría ser útil para diferenciar tumores GIST de otras lesiones como leiomiomas, o leiomiosarcomas…
El TAC con contraste, es el método de elección en pacientes con sospecha de masa abdominal. Suelen ser masas grandes, de crecimiento exofítico, heterogéneas, y vascularizadas. Pueden tener hemorragia, necrosis, quistificación… (38).
Lo mismo ocurre en la enfermedad avanzada: masas irregulares de densidad heterogénea, peritoneales, hepáticas…
Sin embargo, el TAC es incapaz de diferenciar entre las adhesiones inflamatorias y la afectación de órganos vecinos. Así como tampoco metástasis peritoneales menores de 2 cm (1).
En cualquier caso, sirve para diagnóstico y estadiaje de la enfermedad.
En los casos de GIST rectal conocido una RNM aporta más información que el TAC (38).
El PET ofrece información sobre la actividad metabólica a partir del consumo de glucosa. Muestra una imagen total-body, pero tiene una capacidad limitada para valorar el tamaño tumoral. Es útil para calibrar el grado de malignidad, pues a mayor captación de glucosa, mayor actividad metabólica, y por tanto, mayor agresividad. Sirve para diferenciar tumores activos de fibrosis y recidivas de necrosis.
El PET es idóneo para valorar las respuestas tempranas al tratamiento (38).
Sin embargo es una prueba cara y tiene una menor disponibilidad que el TAC.
La conferencia de Consenso de Lugano (38), establece que el PET se debe usar cuando es necesaria una detección precoz de la respuesta tumoral al tratamiento con Imatinib, por ejemplo para considerar una intervención quirúrgica tras la reduccción producida por el fármaco en tumores rectales. Así como también en imágenes equívocas, en las que se sospecha la presencia de metástasis. Aparte de estos casos no es indispensable en todos los pacientes con GIST tras la resección completa.
Por tanto:
TAC proporciona detalles anatómicos del tumor y debe ser utilizado para diagnóstico y estadiaje.
PET puede detectar tumores pequeños y es un indicador fiable de respuesta temprana al tratamiento.
RNM es mejor para tumores rectales.
¿Y en cuanto a la biopsia?
No se alcanzó un consenso de los expertos en cuanto a la necesidad de un diagnóstico preoperatorio mediante biopsias por punción nuclear, obtenidas mediante ecografía endoscópica o percutáneamente.
Si se programa una biopsia preoperatoria, dado que son tumores frágiles y que sangran con facilidad, se prefiere la participación de un equipo multidisciplinario de expertos.
Además, algunos de los expertos, desaconsejan la biopsia abierta intraabdominal debido al riesgo de diseminación tumoral, a menos que existan lesiones hepáticas múltiples.
Por otra parte, cada vez más frecuencia, se requiere de los patólogos que hagan sus diagnósticos, con menor cantidad de tejido. Así, el diagnóstico de GIST en biopsias por aguja o biopsias de mucosa, es relativamente difícil. A no ser que, el tumor sea de muy alto grado, no podremos aportar información pronóstica en una biopsia pequeña. Muchos GIST malignos tienen áreas que parecen benignas, y por tanto, el muestreo puede suponer un problema. Puede ocurrir también que las áreas biopsiadas sean CD117 negativas mientras que otras partes del tumor sean positivas, lo cual conduciría a un error diagnóstico (16).
TRATAMIENTO
La conducta óptima a seguir ha sido un campo de intensa actividad durante los últimos años. La mayoría de los expertos veían la necesidad de intercambiar experiencia y conocimientos actuales y de revisar la situación actual en el campo de los GIST, con el objeto de definir unas directrices para la práctica clínica.
En este sentido, la National Comprehensive Cancer Network (NCCN) estableció en el 2003 una expansión y actualización de las NCCN Practice Guidelines para el tratamiento óptimo de los pacientes con GIST (40).
Y, con el objeto de ampliar estas directrices, se puso en marcha un proyecto semejante bajo los auspicios de la ESMO (European Society of Medical Oncology), celebrándose una reunión en Lugano en Marzo de 2004. Participó un panel de 41 expertos de Europa, Asia, Australia y América, constituido por patólogos, cirujanos y biólogos moleculares.
GIST primario
El tratamiento del GIST primario es la resección completa con márgenes microscópicos libres, con pseudocápsula intacta (pues la rotura puede provocar hemorragia y diseminación). En el caso de intestino y estómago sería correcta una resección segmentaria (38).
En el esófago, duodeno y recto, una resección más amplia. Y resección en bloque si se adhiere a órganos vecinos.
En GIST de epiplon y mesenterio se recomienda resección en bloque de la enfermedad visible.
Debería evitarse la cirugía laparoscópica por el mayor riesgo de rotura tumoral y la siembra peritoneal consiguiente. Sí podría aceptarse en caso de tumores pequeños (<2 cm) e intramurales.
No es necesaria la linfadenectomía puesto que sólo de manera excepcional metastatizan a ganglios linfáticos.
Y, puesto que se considera que todo GIST tiene potencial maligno, deben extirparse todas las lesiones de este tipo, aunque se trate de tumores pequeños intramurales del tubo digestivo.
La supervivencia tras tratamiento de GIST primario es del 50-65% a los 5 años.
Pero, hay que tener en cuenta, que el tamaño tumoral predice la supervivencia, de tal manera que tumores mayores de 10 cm tienen una supervivencia menor, 20% a los 5 años (36).
Asimismo, la supervivencia libre de recidiva se correlaciona con el tamaño tumoral y el índice mitótico. Así, los tumores mayores de 10 cm tienen una tasa de supervivencia del 27%, mientras que los menores de 5 cm del 82% (19).
De igual manera, un índice mitótico alto eleva las posibilidades de recidiva.
El tratamiento con Glivec® tras resección completa de enfermedad metastásica, no se considera adyuvante y entra en el ámbito del uso del Fármaco en EEUU y Europa (38).
El tratamiento adyuvante podría ayudar a erradicar la enfermedad microscópica, pero también puede reducir la eficacia del fármaco en el tratamiento del GIST recidivante y facilitar la aparición de clones resistentes al tratamiento.
La adyuvancia, por tanto, debe circunscribirse a ensayos clínicos.
Actualmente, hay dos ensayos de éstos en Europa. Uno en Fase III realizado por la EORTC junto al French Sarcoma Group, el Italian Sarcoma Group, el Grupo Español de Investigación de Sarcomas (GEIS) y el Australian Gastrointestinal Study Group.
El segundo estudio es un ensayo en fase II aleatorizado, llevado a cabo por el Scandinavian Sarcoma Group con 80 pacientes con riesgo alto de recidiva.
En EEUU, se llevan a cabo otros dos estudios.
En cuanto a la neoadyuvancia, los miembros del panel de expertos de Lugano, acordaron que no había datos que respaldaran el empleo de Glivec neoadyuvante cuando una reducción del tamaño tumoral no va a modificar la cirugía.
Además, dadas las dificultades en evaluar la respuesta tumoral y el riesgo de resistencia primaria, el tratamiento neoadyuvante no debe ser considerado un método de uso habitual. Esta estrategia no se recomienda, por tanto, fuera del marco de los ensayos clínicos.
Sin embargo, el fármaco puede ser usado por equipos multidisciplinarios con experiencia, cuando el objetivo es la cirugía para preservar la función. Esta situación puede ser especialmente frecuente en tumores rectales y esofágicos.
Enfermedad avanzada
Tras la cirugía, y a pesar de una resección aparentemente curativa, se dan hasta un 40-90% de recidivas. A veces por rotura tumoral. Sin embargo, en la mayoría de los pacientes, se produce tras una resección sin complicaciones y a priori completa.
La resección quirúrgica puede ser útil en estos pacientes. Por desgracia, lo que por técnicas de imagen parece un sólo nódulo, suelen ser más en la laparotomía. Varios nódulos o incluso una sarcomatosis manifiesta. Los tumores recidivantes se limitan a la región del tumor primario (25%) o se localizan difusamente por todo el abdomen. Al igual que los GIST primarios, los nódulos peritoneales recidivantes suelen posarse sobre la superficie del intestino, epiplon, mesenterio o la pared abdominal, y no invaden significativamente las estructuras circundantes. Por lo tanto, a menudo se pueden eliminar con resecciones limitadas (38,41).
Las metástasis hepáticas podrían tratarse mediante resección, quimioembolización o incluso ablación por radiofrecuencia. Sin embargo, son habitualmente multifocales, y ello dificulta la cirugía.
En cualquier caso, debe intentarse la resección completa de las recidivas, si es una sola lesión, o muchas de pequeño volumen, en múltiples localizaciones superficiales.
No están justificadas las resecciones de múltiples órganos abdominales, ni la disminución del tamaño del tumor. A excepción de evitar hemorragias y/o obstrucciones.
Y, por supuesto, está contraindicada en pacientes con mal estado funcional.
En todos estos casos, el tratamiento de primera línea es el tratamiento médico con Glivec®, que debe ser inmediato, según las directrices de la reunión de Lugano.
Tratamiento médico: Glivec®
Glivec® compite con el ATP en la fijación del dominio de la tirosina quinasa, e inhibe la activación y fosforilación del mismo (42).
Hirota y colaboradores, en 1998, fueron los primeros en describir la presencia de mutaciones KIT en los GIST. Esta descripción abrió la puerta del uso posterior de Glivec® en estos tumores, que en principio estaba diseñado para la LMC.
La era del Glivec en el tratamiento de GIST se inició con un estudio de prueba de concepto en un único paciente. Una mujer con un tumor GIST gástrico, con mutación en el exon 11 del gen KIT (6). Un tumor metastásico y recidivante, y en progresión, a pesar de cirugía y tratamiento quimioterápico.
En los dos primeros meses se observó una reducción del volumen tumoral del 50% y a los 18 meses esta reducción era del 78%.
A las 4 semanas, en el PET, se observó una disminución de la captación de glucosa muy significativa.
A partir de aquí, la historia del Glivec® ha sido la más rápida del campo de la Oncología (43,44).
Comenzaron estudios en Fase I con 40 pacientes (12), 36 de ellos con GIST. A dosis de 400-1.000 mg. Se valoraron efectos adversos: náuseas, vómitos, edema…
Posteriormente, se realizaron estudios en fase II, por investigadores de EEUU y Finlandia (45). En total, el 53,7% de los pacientes mostraron una respuesta parcial objetiva a Glivec® y un 27,9% mostraron enfermedad estable.
Tras quedar patente la eficacia del Glivec®, se pusieron en marcha estudios en Fase III, y antes de que hubiera resultados, la FDA americana aprobó el uso del fármaco.
Se compararon dosis de 400 y 800 mg, sin placebo (quedó ya descartado tras la fase I). Un ensayo dirigido por la EORTC (41), tenía como variable la supervivencia libre de progresión e incluyó 946 pacientes. Se observaron respuestas parecidas para ambas dosis, tanto en parámetros de eficacia como de toxicidad. La respuesta parcial fue del 44,7% para dosis de 400 mg, y del 47,2% para 800 mg. Y enfermedad estable fue de 32,7% para dosis 400 mg y 33,3% para 800 mg. Es decir 82% de respuesta en dosis de 400 y 84% en dosis de 800 mg. La supervivencia libre de progresión a 12 meses presentó unos porcentajes de 50 y 58% respectivamente.
En el estudio estadounidense (US S0033) participaron 746 pacientes, y los resultados fueron similares.
Queda patente que, la dosis óptima es de 400 mg. En ambos estudios se permitió escalada de dosis de 400 a 800 mg en caso de progresión.
Además, varios estudios han demostrado que el tipo de mutación se correlaciona con el curso clínico tras tratamiento con Glivec®. Así, Heinrich, en el estudio CSTIB222 en fase II, demostró que pacientes con mutaciones exon 11 tenían una tasa de respuesta parcial significativamente superior (83,5%), frente a los pacientes con mutaciones en el exón 9 (48,7%), o aquellos sin mutación detectable (0%) (46).
La respuesta parcial confirmada se alcanza con 400 mg en 67% de pacientes después de 34 meses de seguimiento. Y la tasa de respuesta aumenta a medida que aumenta el tiempo de seguimiento.
La duración del tratamiento debe ser de por vida. La interrupción del tratamiento provoca un crecimiento tumoral acelerado y no se debe realizar fuera de ensayos clínicos. En un estudio en fase III aleatorizado (47), tras 12 meses de tratamiento se randomizó a continuar o discontinuar el tratamiento. En los pacientes que interrumpieron el tratamiento se registró un intervalo de progresión de 6 meses. Mientras que ninguno de los que continuó mostró progresión hasta los 7 meses. Se suspendió por tanto la randomización. Esto, se observó en imágenes del PET, como un aumento de la captación. Por tanto, incluso en tumores donde existe progresión parcial, la terapia con Glivec® debería seguirse, si la mayoría de la carga tumoral está bajo control.
El tratamiento se seguirá hasta la progresión, intolerancia o rechazo del paciente (38).
En respuesta al tratamiento, las lesiones hepáticas adoptan a menudo un patrón quístico en el TAC.
Histológicamente, se corresponde a una degeneración mixohialina en la que se ven núcleos apoptóticos. Pero podría haber algunas células positiva para c-KIT restantes, en fase latente o células GIST en proliferación lenta que podrían persistir durante varios meses en estas lesiones (48).
La evaluación de la respuesta al tratamiento mediante técnicas de imagen se basan en disminución del tamaño, disminución de nódulos tumorales, calcificación, quistificación…
Sin embargo, el TAC empieza a detectar variaciones de tamaño a los 3-6 meses. Incluso puede que los tumores aumenten de tamaño, en la fase inmediata posterior al tratamiento (38), a pesar de la mejoría sintomática. Puede deberse a hemorragia intratumoral, edema o degeneración mixoide.
Podrían utilizarse otros criterios para evaluar la respuesta, como son, el cambio de densidad tumoral o la disminución del realce de contraste. Así, los tumores que responden pasan de ser heterogéneos e hipervasculares a homogéneos e hipoatenuados (19).
La respuesta temprana al tratamiento puede ser evaluada mediante PET, que detecta cambios en la captación tras 4 semanas. Es una técnica sensible, aunque es cara, y de escasa disponibilidad.
De elección por tanto, sería el TAC, salvo cuando sea necesario un seguimiento a corto plazo (1-2 semanas), por ejemplo para tomar una decisión quirúrgica en los pacientes con tumores «marginalmente extirpables» (38).
La resistencia al tratamiento es bien conocida (49,50). Y puede ser:
Primaria. Un 15% o menos de pacientes presentan una resistencia primaria. Tiene una progresión rápida y nunca se benefician de Glivec (46).
Adquirida o secundaria. Pacientes que han mostrado una estabilización inicial o respuesta a enfermedad durante más de 3 meses y luego presentan progresión.
La resistencia primaria es generalmente multifocal. Estos tumores presentan a menudo KIT de tipo salvaje, mutaciones en exon 9 de KIT o bien una mutación PDGFRA con mutación D842V (1,36,38,41,51).
La resistencia adquirida aparece después del periodo de 6 meses. Puede ser parcial (52) o multifocal.
En la actualidad existen otras opciones terapéuticas en el caso de tumores resistentes:
SU11248 (53,54): inhibidor de los Receptores de tirosina kinasa PDGFRA, VEGFR, KIT y FLT3 (23).
AMG706: presenta especificidad contra KIT y VEGFR (36,41).
RAD001 (Everolimus): en combinación con Glivec.
Bevacizumab: en combinación con Glivec.
PKC412: en combinación con Glivec (40).
Muchos tumores expresan KIT, pero sólo en algunos se observa la mutación del gen KIT o PDGFRA.
Sihto (55), en un estudio de 334 tumores de diferentes tipos, con expresión inmunohistoquímica de c-KIT. Observó mutación KIT únicamente en 17 tumores, todos ellos GIST.
Otros tumores que pueden expresar KIT incluyen: neuroblastomas, leucemia mieloide aguda, carcinoma de mama, carcinoma de ovario, carcinoma adenoide quístico, carcinoma tiroideo.
El papel de KIT en estas neoplasias no se conoce pero, se cree, que en ausencia de mutación KIT, la expresión de la proteína KIT pudiera estar relacionada con amplificaciones del gen o la presencia de múltiples copias del cromosoma 4. Estos amplicons pueden contener PDGFRA. Porque KIT y PDGFRA están estrechamente relacionados en el cromosoma 4q12 (56).
Se han realizado estudios en el tratamiento de tumores como Dermatofibrosarcoma protuberans o tumores desmoides (48,57,58).
ESTUDIO RETROSPECTIVO HOSPITAL DE CRUCES (1980-2003)
Se realizó un estudio retrospectivo de 352 casos de neoplasias estromales del TGI, peritoneo, retroperitoneo y mesenterio.
Se estudiaron 57 GIST, 215 Leiomiomas, 43 Leiomiosarcomas, 10 Leiomioblastomas, 12 Sarcomas, 9 Schwannomas, 1 Sarcoma fusocelular, y otros (1 Mixosarcoma, 2 Lipomixosarcomas, 2 Fibrosarcomas).
De todos ellos, 149 cumplían los criterios diagnósticos de GIST.
El 32% de los GIST fueron tumores de muy bajo riesgo, el 35% de bajo riesgo, un 22% de riesgo intermedio, y un 11% de alto riesgo.
De los 97 casos de bajo o muy bajo riesgo, el 17% recidivaron, todos ellos de bajo riesgo, ninguno de los de muy bajo riesgo.
47 casos recidivaron, siendo la localización más común el peritoneo. De ellos, el 17% eran de bajo riesgo, el 50% de riesgo intermedio, y un 33% de riesgo alto.
19 casos metastatizaron, preferentemente al hígado. El 26% eran de muy bajo riesgo, el 24% de bajo riesgo, el 29% de riesgo intermedio, y el 21% de riesgo alto.
Se observó, por tanto, una falta de correspondencia, entre los rasgos histopatológicos de riesgo, y el comportamiento clínico, en un total de 41 casos.
CONCLUSIONES
GIST es un sarcoma poco frecuente, sin embargo la mayoría de los sarcomas del TGI son GIST.
Su incidencia es mucho más elevada de lo estimado.
La mutación del gen KIT es un evento oncogénico precoz, y la presencia del gen mutado per se no tiene importancia pronóstica.
Existen GIST c-KIT negativos, la mayoría de los cuales tiene mutaciones del gen de PDGFRA.
En caso de un cuadro morfológico de GIST y negatividad para CD117, es necesario investigar las mutaciones de KIT y PDGFRA.
Ningún GIST debe ser considerado benigno.
Glivec® es efectivo en el tratamiento de los tumores GIST metastásicos e irresecables.
Actualmente se llevan a cabo estudios en Fase II/III para determinar su utilidad en adyuvancia y neoadyuvancia.
La interrupción del tratamiento está asociada a alto riesgo de recidiva, por lo que el tratamiento debe ser de por vida.
Aunque el pronóstico ha mejorado, no es una cura, un 10-35% presentan resistencia primaria al tratamiento, y en un 50% de los avanzados se observa una resistencia secundaria.
Existen opciones terapéuticas en estudio: SU11248, RAD001 y otras.
BIBLIOGRAFÍA
Saund MS, Demetri GD, Ashley SW. Gastrointestinal stromal tumors (GISTs). Curr Opin Gastroenterol 2004; 20: 89-94.
Bucher P, Villiger P, Egger J-F, et al. Management of gastrointestinal stromal tumors: from diagnosis to treatment. Swiss Med Wkly 2004; 134: 145-53.
Miettinem M, Lasota J. Gastrointestinal stromal tumors (GISTs): definition, ocurrence, pathology, differential diagnosis, and molecular genetics. Pol J Pathol 2003; 54: 3-24.
Kinblom L-G, Remotti HE, Aldenborg F, et al. Gastrointestinal Pacemeaker cell tumor (GIPACT). Gastrointestinal stromal tumors show phenotypic characteristics of interstitial cells of Cajal. Am J Pathol 1998; 152: 1259-69.
Corless CL, Fletcher JA and Heinrich MC. Biology of gastrointestinal stromal tumors. J Clin Oncol 2004; 22: 3813-25
Joenssu H, Roberts P, Sarlomo-Rikala M, et al. Effect of the Tyrosine Kinase inhibitor STI571 in a patient with metastatic gastrointestinal stromal tumor. N Engl J Med 2001; 344: 1052-6.
Nilsson B, Bümming P, Meiss-Kinblom J M, et al. Gastrointestinal stromal tumors: the incidence, prevalence, clinical course, and prognostication in the preimatinib mesylate era. A population-based study in Western Sweden. Cancer 2005; 103: 821-9.
Miettinem M, Majidi M, Lasota J. Pathology and diagnostic criteria of gastrointestinal stromal tumors (GISTs): a review. Eur J Cancer 2002; 38, Suppl. 5: S39-S51.
Fletcher CDM. Berman JJ, Corless C, et al. Diagnosis of gastrointestinal stromal tumors: A consensus approach. Hum Pathol 2002; 33: 459-65.
Ortega Medina L. Tumores del estroma gastrointestinal (comunicación personal). Curso de Patología Oncológica. Sevilla noviembre 2004.
Fukasawa T, Chong J-M, Sakurai S, et al. Allelic loss of 14q and 22q, NF2 mutation, and genetic instability occur independently of c-KIT mutation in gastrointestinal stromal tumor. Jpn J Cancer Res 2000; 91: 1241-9.
van Oosterom AT, Judson I, Stroobants S, et al. The Lancet 2001; 358: 1421-3.
West RB, Corless CL, Chen X, et al. The Novel marker, DOG1, is expressed ubiquituosly in gastrointestinal stromal tumors irrespective of KIT or PDGFRA mutation status. Am J Surg Pathol 2004; 165: 107-13.
Medeiros F, Corless CL, Duensing A, et al. KIT-Negative gastrointestinal stromal tumor. Proof of concept and Therapeutic implications. Am J Surg Pathol 2004; 28: 889-94.
Motegi A, Sakurai S, Nakayama H, et al. PKC theta, a novel immunohistochemical marker for gastrointestinal stromal tumors (GIST), especially useful for identifying KIT-negative tumors. Pathology International 2005; 55: 106-12.
Greenson JK. Gastrointestinal stromal tumor. (Comunicación personal). Curso patología digestiva. Hospital del Mar. Barcelona, enero 2006.
Miettinem M, El-Rifai W, Lasota J, et al. Evaluation of malignancy and prognosis of gastrointestinal stromal tumors. Hum Pathol 2002; 33: 478-83.
Miettinem M, Sobon LH, Lasota J: gastrointestinal stromal tumors of the stomach. Am J Surg Pathol 2005; 29: 52-68.
Singer S, Rubin BP, Lux ML, et al. Prognostic value of KIT mutation Type, mitotic Activity, and histologic subtype in gastrointestinal stromal tumors. J Clin Oncol 2002; 20: 3898-905.
Feakins RM. The expression of p53 and bcl-2 in gastrointestinal stromal tumors is associated with anatomical site, and p53 expression is associated with grade and clinical outcome. Histopathol 2005; 46: 270-9.
Panizo-Santos A, Sola I, Vega F, et al. Predicting risk of gastrointestinal stromal tumors: role of cell proliferation and cell cycle regulatory proteins. Int J Surg Pathol 2000; 8: 133-44.
Montgomery E, Abraham SC, Fisher C, et al. CD44 loss in gastric stromal tumors as a prognostic marker. Am J Surg Pathol 2004; 28: 168-77.
Scheider-Stock R, Boltze C, Lasota J, et al. Loss of p16 protein defines high-risk patients with gastrointestinal stromal tumors: a tissue microarray. Clin Cancer Res 2005; 11: 638-45.
Han Lee J, Zhang X, Yong Jung W, Chae JS, Park J-J, Kim I. DNA ploidy and c-KIT mutation in gastrointestinal stromal tumors. World J Gastroenterol 2004; 10: 3475-9.
Lasota T, Dansonka-Mieszkowska A, Stachura T, et al. Gastrointestinal stromal tumors with internal tandem duplications in 3´ end of KIT yuxtamembrane domain occur predominantly in stomach and generally seem to have a favourable course. Mod Pathol 2003; 16: 1257-64.
Yi ES, String CR, Piao Z, et al. Epithelioid stromal tumor with PDGFRA activating mutation and immunoreactivity. Appl Immunohistochem Mol Morphol 2005; 13: 157-61.
Martin J, Poveda A, Llombart-Bosch A, et al. Deletions affecting codons 557-558 of the c-KIT gene indicate poor prognosis in patients with completely resected gastrointestinal stromal tumors: A study by the Spanish Group of Sarcoma Research (GEIS). J Clin Oncol 2005; vol 23, No25: 6190-8.
Heinrich MC, Rubin BP, Longley BJ, et al Biology and aspects of gastrointestinal stromal tumors: KIT activation and cytogenetic alterations. Hum Pathol 2002; 33: 484-95.
Rubin BP, Singer S, Tsao C, et al. KIT activation is a ubiquitous feature of gastrointestinal stromal tumors. Cancer Res 2001; 61: 8118-21.
Lasota J, Jasinsky M, Sarlomo-Rikala M, Miettinem M. Mutation in exon 11 of c-KIT occur preferentially in malignant versus benign gastrointestinal stromal tumors and do not occur in Leiomyomas or Leiomyosarcomas. Am J Pathol 1999; 154: 53-60.
Corless CL, McGreevey AH, Town A, et al. Kit mutations are common in incidental gastrointestinal stromal tumors one centimeter or less in size. Am J Pathol 2002; 160: 1567-72.
Dirnhofer S. Tyrosine kinase family of receptors and their mutations: Molecular pathology of GIST. (Comunicación personal). Encuentro Internacional sobre la patología del GIST. Valencia 10 septiembre 2004.
Rubin BP. Gastrointestinal stromal tumors: an update. Histopathology 2006; 48: 83-96.
Heinrich MC, Blanke CD, Druker BJ, et al. Inhibition of KIT Tyrosine Kinase Activity: A novel molecular approach to the treatment of KIT-positive malignancies. J Clin Oncol 2002; 20: 1692-703.
Corless CL, Schroeder A, Griffith D, et al. PDGFRA mutations in gastrointestinal stromal tumors: frequency, spectrum, and in vitro sensitivity to Imatinib. J Clin Oncol 2005; 10: 5357-64.
van der Zwan S, DeMatteo RP. Gastrointestinal stromal tumor: 5 years later. Cancer 2005; 104: 1781-8.
El-Rifai W, Sarlomo-Rikala M, Andersson LC, at al. Different patterns of DNA copy number changes in gastrointestinal stromal tumors, leiomiomas, and schwannomas. Hum Pathol 1998; 29: 476-81.
Blay J-Y, Bonvalot S, Casali P, Choi H, et al. Reunión de consenso sobre el tratamiento de los tumores estromales gastrointestinales. Informe de los GIST Consensus Conference del 20-21 de Marzo de 2004, bajo los auspicios de la ESMO. Ann Oncol 2005; 16: 566-78.
El GIST modelo de investigación oncológica moderna. Sesión educacional. V Congreso Nacional FESEO. Valencia, 17-19 noviembre 2004.
Demetri GD, Benjamin RS, Blanke C, et al. Optimal management of patients with gastrointestinal stromal tumors. Expansion and update of NCCN Clinical Practice Guidelines. JNCCN 2004; 2 Suppl 1: S1-S26.
Von Mehren M, Watson JC. Gastrointestinal stromal tumors. Hematol Oncol Clin N Am 2005; 19: 547-64.
Buchdunger E, O´Reilly T, Wood J. Pharmacology of Imatinib (STI571). Eur J Cancer 2002; 38 Suppl 5: S28-S36.
De Matteo RP, Heinrich MC, El-Rifai W, et al. Clinical management of gastrointestinal stromal tumors: Before and after STI-571. Hum Pathol 2002 33; 5: 466-77.
Joensuu H, Fletcher C, Dimitrijevic S, Silberman S, et al. Tratamiento de los tumores del estroma gastrointestinal. Lancet Oncol 2002; 3: 655-64.
Demetri GD, von Mehren M, Blanke CD, et al. Efficacy and safety of Imatinib mesylate in advanced gastrointestinal stromal tumors. N Engl J Med 2002; 347: 472-80.
Heinrich MC, Corless CL, Demetri GD, et al. Kinase mutations and Imatinib response in patients with metastatic gastrointestinal stromal tumor. J Clin Oncol 2003; 21: 4342-9.
Blay J-Y, Berthaud P, Perol D, et al. Continuous vs intermittent Imatinib treatment in advanced GIST after one year: A prospective randomized phase III trial of the French Sarcoma Group. Proc Am Soc Clin Oncol 2004; 23: 815.
Heinrich MC, McArthur GA, Demetri GD, et al. Clinical and molecular studies of the effect of Imatinib on advanced aggressive fibromatosis (desmoid tumor). J Clin Oncol 2006; 24: 1195-203.
Debiec-Richter M, Cools J, Dumez H, et al. Mechanisms of resistance to imatinib mesylate in gastrointestinal stromal tumors and activity of the PCK412 inhibitor against imatinib-resistant mutants. Gastroenterol 2005; 128: 270-9.
Heinrich MC, Corless CL, Blanke CD, et al. Molecular correlates of Imatinib resistance in gastrointestinal stromal tumors. J Clin Oncol 2006; 24: 1-11.
Heinrich MC, Corless CL, Duensing A, et al. PDGFRA activating mutations in gastrointestinal stromal tumors. Science 2002; 299: 708-10.
Shankar S, van Sonnenberg E, Desai J, et al. Gastrointestinal stromal tumor: new nodule-within-a-mass pattern of recurrence after partial response to Imatinib mesylate. Radiology 2005; 235: 892-8.
Prenen H, Cools J, Mentens N et al. Efficacy of the kinase inhibitor SU11248 against gastrointestinal stromal tumor Mutants Refractory to Imatinib Mesylate. Clin Cancer Res 2006; 12: 2622-7.
Tzen C-Y, Mau B-L. Analysis of CD117 negative gastrointestinal stromal tumors. World J Gastroenterol 2005; 11: 1052-5.
Sihto H, Sarlomo-Rikala M, Tynninen O, et al. KIT and Platelet-Derived Growth Factor Receptor Alpha tyrosine kinase gene mutations and KIT amplifications in human solid tumors. J Clin Oncol 2005; 23: 49-57.
Lasota J, Stachura J, Miettinem M. GISTs with PDGFRA exon 14c mutations represent subset of clinically favourable gastric tumors with epithelioid morphology. Lab Invest 2006; 86: 94-100.
Mace J, Biermann JS, Sondak V, et al. Response of extraabdominal desmoid tumors to therapy with Imatinib Mesylate. Cancer 2002; 95: 2373-9.
Sjöblom T, Shimizu A, O`Brien K, et al. Growth inhibition of Dermatofibrosarcoma Protuberans tumors by the Platelet-derived growth factor receptor antagonist STI571 through induction of apoptosis. Cancer Res 2001; 61:5778-83.